. 在某澄清、透明的黄色溶液中,可能含有NH4+、Fe3+、Ba2+、Al3+、SO42-、HCO3-、I- Cl-离子。进行下述实验(所加试剂均过量)。
(1) 沉淀 A的化学式是 ,气体A的化学式是 ;
(2)待测液中一定存在 ;一定不存在 _______ 用离子方程式表示上述离子一定不存在的原因 。
(3)写出溶液C与过量氨水反应的离子方程式 。
(4)若气体A、沉淀A、沉淀D的物质的量各为1mol,则SO42-的物质的量为: mol
以黄铁矿为原料制硫酸产生的废渣中含Fe2O3、SiO2、Al2O3、CaO、MgO等。现以此废渣制备铁红(Fe2O3)的过程如下。此浓度时,部分阳离子以氢氧化物形式沉淀时溶液的pH见右表。
(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式是。
(2)还原过程中加入FeS2是将溶液中的Fe3+还原为Fe2+,而本身被氧化为SO42-,写出离子方程式:。
(3)氧化过程中通入空气和加入NaOH是为了将溶液中的铁元素充分转化为沉淀而析出,写出总反应的离子方程式:。
(4)为了确保铁红的质量,氧化过程需要调节溶液pH的范围为≤pH<。
(5)若NaOH加入过量,所的铁红产品中有其它杂质,但可能无Al2O3,其原因是(用离子方程式表示):。
有一透明溶液,已知其中可能含有Mg2+、Cu2+、Fe2+、Al3+、NH4+、K+、Cl-、
HCO3-、SO42-。当加入一种淡黄色粉末状固体物质时,有刺激性气味的混和气体放出,同时生成白色沉淀。当加入0.4mol淡黄色粉末时,共收集到0.3mol混和气体,且此时生成的沉淀最多。此后继续加入淡黄色粉末时,沉淀量逐渐减少,至加入0.45mol粉末后,沉淀量由0.3mol减少至0.2mol,再加入粉末后,沉淀就不再减少。由此实验现象及数据判断:
(1)淡黄色粉末的名称为;
(2)溶液中肯定有离子,肯定没有离子,可能有________离子;
(3)写出下列反应方程式
①淡黄色粉末与水反应;
②产生刺激性气味气体的离子方程式;
③加入淡黄色粉末的物质的量由0.4mol至0.45mol时,沉淀部分消失,反应的离子方程式为;
(4)溶液中阳离子的物质的量之比为(H+及没有确定的离子除外)。
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、Al3+和五种阴离子Cl-、OH-、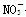 、
、 、X中的一种。
、X中的一种。
(1)某同学通过比较分析,认为无须检验就可判断其中必有的两种物质是________和________。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体,则X为________(填字母)。
A.Br-B. C.CH3COO-D.
C.CH3COO-D.
(3)将19.2 g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式__________________,若要将Cu完全溶解,至少加入H2SO4的物质的量是____________________。
(4)E溶液与氢碘酸反应时可生成棕色物质,该反应的离子方程式为______________。
部分中学化学常见元素原子结构及性质如下表所示:
| 序号 |
元素 |
结构及性质 |
| ① |
A |
A单质是生活中的常见金属,它有两种氯化物,相对分子质量相差35.5 |
| ② |
B |
B原子最外层电子数是内层电子总数的1/5 |
| ③ |
C |
C是常见化肥的主要元素,单质常温下呈气态 |
| ④ |
D |
Dm+与Cn-的核外电子排布相同,且Dm+半径在同周期中离子半径最小 |
| ⑤ |
E |
通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 |
| ⑥ |
F |
F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
(1)A元素在周期表中的位置为_______________________________________。
(2)B与C形成的化合物的化学式为________,写出此化合物与水反应的化学方程式。
(3)①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,请写出用电子式表示Y形成过程的式子______________________________________。
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的水溶液显________性(填写“酸”、“碱”或者“中”),N的结构式为__________________________。
(4)C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱:_____________。
(5)有人认为B、D的单质用导线连接后插入NaOH溶液中可以形成原电池,你认为是否可以,若可以,试写出负极的电极方程式(若认为不行可不写): ________________。
以铬铁矿(主要成分是FeO·Cr2O3,含少量MgCO3、Al2O3、SiO2等)为原料制取铬酸钠(Na2CrO4)晶体的工艺流程如下:
已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以 形式存在且易氧化;②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下。
形式存在且易氧化;②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下。
| 阳离子 |
Fe3+ |
Fe2+ |
Mg2+ |
Al3+ |
Cr3+ |
| 开始沉淀时的pH |
2.7 |
7.6 |
9.0 |
—— |
—— |
| 沉淀完全时的pH |
3.7 |
9.6 |
11.0 |
8 |
9(>9溶解) |
(1)流程中两次使用了H2O2,分别写出反应的离子方程式:__________________、_________________。
(2)加入NaOH调节溶液的pH=8时,被除去的离子是________;调节溶液的pH>11时,被除去的离子是________。
(3)“调pH=8”和“调pH>11”中间的“过滤”步骤不能省略,为什么?____________。
(4)流程图中 内的操作是______________________。
内的操作是______________________。