下列说法中,正确的是
| A.常温常压下,活泼金属与盐酸反应置换生成1摩H2,发生转移的电子数为1NA |
| B.22.4 L氢气中,一定含有2 mol氢原子 |
| C.在常温常压下,28g CO和N2的混合气体中含有的分子数为1NA |
| D.80gNaOH溶解在1 L水中,得到溶液的物质的量浓度为2mol/L |
下列离子方程式正确的是
| A.在碳酸氢钙溶液中加入少量盐酸:Ca2++2HCO3-+2H+→CO2↑+2H2O+CaCO3↓ |
| B.硫酸铁溶液与氢氧化钡溶液:Fe3++SO42-+Ba2++3OH-→Fe(OH)3↓+BaSO4↓ |
| C.次氯酸钙溶液中通入足量二氧化硫:Ca2++ClO-+SO2+H2O→CaSO4↓+Cl-+2H+ |
| D.氢氧化钠溶液中通入过量二氧化碳:OH-+CO2→HCO3- |
以石化产品乙烯、丙烯为原料合成厌氧胶的流程如下。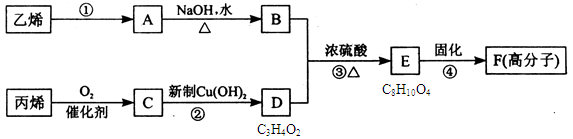
关于该过程的相关叙述正确的是
| A.反应④的反应类型是加聚 | B.物质A是卤代烃 |
| C.物质B催化氧化后可以得到乙醛 | D.1mol物质D最多可以消耗2molNaOH |
阿佛加德罗常数用NA表示,下列叙述正确的是
| A.室温时,1LpH=2的NH4Cl溶液中水电离出10-12molH+ |
| B.常温常压下,46gNO2含3NA个原子 |
| C.1molLiAlH4在125℃完全分解成LiH、H2、Al,转移电子3NA |
| D.12g石墨含有4NA个自由移动的电子 |
下列离子或物质组能大量共存,且满足相应条件的是
| 选项 |
离子或物质 |
条件 |
| A |
Na+、K+、Cl-、SO42- |
c(Na+)+c(K+)=c(SO42-)+ c(Cl-) |
| B |
Fe3+、SO32-、Cl- |
加入NaOH溶液,产生红褐色沉淀 |
| C |
Ba+、HCO3-、Cl-、H+ |
加入氨水产生沉淀 |
| D |
SO2、O2、NO2 |
通入足量NaOH溶液后,可能会没有任何气体剩余 |
在密闭容器中进行反应:2A(g)+B(g) 3C(g)+Q(Q>0)。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
3C(g)+Q(Q>0)。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是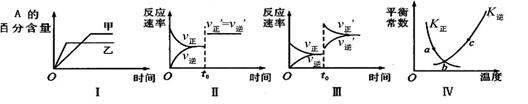
| A.图I表示温度对化学平衡的影响,且甲的温度较高 |
| B.图Ⅱ表示t0时刻缩小容器体积对反应速率的影响 |
| C.图Ⅲ表示t0时刻增大B浓度对反应速率的影响 |
| D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |