化学平衡常数K的数值大小是衡量化学反应进行程度的标志,在常温下,下列反应的平衡常数的数值如下:
2NO(g) N2(g)+O2(g) K1=1×1030
N2(g)+O2(g) K1=1×1030
2H2(g)+O2(g) 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081
2CO2(g) 2CO(g)+O2(g) K3=4×10-92
2CO(g)+O2(g) K3=4×10-92
以下说法正确的是 ( )
| A.常温下,NO分解产生O2的反应的平衡常数表达式为K1=c(N2)·c(O2) |
| B.常温下,水分解产生O2,此时平衡常数的数值约为5×10-80 |
| C.常温下,NO、H2O、CO2三种化合物分解放出O2的倾向由大到小的顺序为NO>H2O>CO2 |
| D.以上说法都不正确 |
随着各地“限牌”政策的推出,电动汽车成为汽车届的“新宠”。特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如图,A 极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许特定的离子通过,电池反应式LixC6+Li1﹣xCoO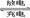 C6+LiCoO2。下列说法不正确的是
C6+LiCoO2。下列说法不正确的是
| A.据题意分析可知该隔膜只允许Li+通过,放电时 Li+从左边流向右边 |
| B.充电时,A为阴极,发生还原反应 |
| C.放电时,B为正极,电极反应式为:Li1﹣xCoO2+xLi++xe﹣=LiCoO2 |
| D.废旧钴酸锂(LiCoO2)电池进行“放电处理”让Li+进入石墨中而有利于回收 |
下列表示化学反应的离子方程式,其中正确的是
A.NH4HSO3溶液与足量NaOH溶液共热:NH4++HSO3-+2OH- NH3↑+SO32-+2H2O NH3↑+SO32-+2H2O |
| B.向氯化铝溶液中加入过量氨水:Al3+ + 4NH3·H2O=AlO2- + 4NH4+ +2H2O |
| C.用盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性: 2 MnO4-+6H++ 5H2O2=2Mn2++5 O2 ↑+ 8H2O |
D.用石墨电极电解饱和MgCl2溶液:2Cl-+2H2O H2↑+ Cl2↑ + 2OH- H2↑+ Cl2↑ + 2OH- |
亚氯酸钠是一种高效氧化剂漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2﹣、Cl﹣等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.经测定,25℃时各组分含量随pH变化情况如图所示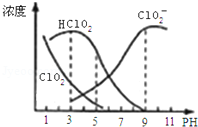
(Cl﹣没有画出).则下列分析正确的是
| A.亚氯酸钠在酸性条件下较稳定 |
| B.25℃时,HClO2的电离平衡常数的数值Ka=10﹣6 |
| C.pH越大,该漂白剂的漂白性能越好 |
| D.25℃,pH=3时,NaClO2溶液中:c(Na+)+(H+)=c(ClO2-)+c(OH-) |
常温下,下列溶液中,能大量共存的一组离子是
| A.pH=1的溶液中:NH4+、Fe2+、SO42-、Cl- |
| B.通入SO2气体的溶液中:Ca2+、I-、ClO-、NO3- |
| C.c(Fe3+)=" 0.1" mol•L-1的溶液中:Na+、I-、SCN-、SO42- |
| D.由水电离出的c(H+)=1.0×10-13mol•L-1的溶液中:Na+、HCO3-、Cl-、Br- |
氨基钠和氢化钠与水反应的化学方程式如下:①NaNH2+H2O=NaOH+NH3↑
②NaH+H2O==NaOH+H2↑,下列叙述正确的是
| A.氨基钠和氢化钠与盐酸反应都只生成一种盐 |
| B.方程式②中,每生成1mol H2转移1 mol电子 |
| C.氨基钠和氢化钠的晶体中都只含离子键 |
| D.方程式①中,氨基钠是还原剂 |