玻璃的主要成分之一是二氧化硅,赏心悦目的雕花玻璃是用下列物质中的一种对玻璃进行刻蚀而制成的。这种物质是( )
| A.盐酸 | B.氢氟酸 | C.烧碱 | D.纯碱 |
下列有关化学用语表示正确的是
A.过氧化钠的电子式: |
B.质子数为35、中子数为45的溴原子: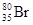 |
C.硫离子的结构示意图: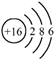 |
D.间二甲苯的结构简式: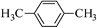 |
下列物质的分类正确的是
| 碱 |
酸 |
盐 |
碱性氧化物 |
酸性氧化物 |
|
| A |
Na2CO3 |
H2SO4 |
NaOH |
SO2 |
CO2 |
| B |
NaOH |
HCl |
NaCl |
Na2O |
NO |
| C |
KOH |
HNO3 |
CaCO3 |
CaO |
Mn2O7 |
| D |
NaOH |
HCl |
CaF2 |
Na2O2 |
SO2 |
N2的结构可以表示为 ,CO的结构可以表示为
,CO的结构可以表示为 ,其中椭圆框表示π键,下列说法中不正确的是
,其中椭圆框表示π键,下列说法中不正确的是
| A.N2分子与CO分子中都含有叁键 | B.CO分子中有一个π键是配位键 |
| C.N2与CO互为等电子体 | D.N2与CO的化学性质相同 |
共价键、离子键和范德华力是构成物质粒子间的不同作用方式,下列物质中,只含有上述一种作用的是
| A.干冰 | B.氯化钠 | C.氢氧化钠 | D.碘 |
美国“海狼”号潜艇上的核反应堆内使用了液体铝钠合金作载热介质,下列关于Al、Na原子结构的分析中正确的是
| A.原子半径:Al>Na | B.第一电离能:Al>Na |
| C.电负性:Na>Al | D.基态原子未成对电子数:Na>Al |