标准状况下,1.68L无色可燃气体在足量氧气中完全燃烧。若将产物通入足量澄清石灰水,得到的白色沉淀质量为15.0g;若用足量碱石灰吸收燃烧产物,增重9.3g。
(1)计算产物中水的质量。
(2)若原气体是单一气体,通过计算推断它的分子式。
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式(写三组)。
某空气污染监测仪是根据SO2和Br2的定量反应来测定空气中SO2含量的。参加反应的溴,来自一个装满酸性(H2SO4)KBr溶液的电解槽阳极上的氧化反应,电解槽的阳极室与阴极室是隔开的。当测量某地区空气中SO2含量时,空气(经过除尘)以1.5×10-4 m3·min-1的流速进入电解槽的阳极室,电流计显示每分钟通过电子是5.136×10-9 mol,此条件下能保持溴浓度恒定并恰好与SO2完全反应。设被测空气中不含其他能与溴反应的杂质。
(1)写出此监测过程中发生的主要反应的化学方程式。
(2)计算该地区空气中SO2的含量(g·m-3)(保留两位小数)。
用Pt电极电解浓度为17%的饱和硝酸银溶液,当金属银完全析出时,阳极上放出5.6 L气体(标准状况),电解后溶液的密度为1.038 g·cm-3。试计算:
(1)电解前原硝酸银溶液的总质量是多少?电解析出的银多少克?
(2)电解前硝酸银的溶解度是多少?
(3)电解后所得溶液的质量分数和物质的量浓度各为多少?
有电解装置如图4-37。图中B装置盛1 L 2 mol·L-1 Na2SO4溶液,A装置中盛1 L 2 mol·L-1 AgNO3溶液。通电后,润湿KI淀粉试纸的C端变蓝色,电解一段时间后,试回答: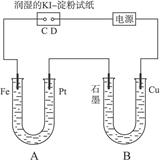
图4-37
(1)A中发生反应的化学方程式为______________________________。
(2)在B中观察到的现象是_________________________。
(3)室温下,若从电解开始到时间为t时,A、B装置中共收集到气体0.168 L(标准状况),若电解过程中无其他副反应发生,且溶液体积变化忽略不计,则在t时,A溶液的pH为_______。
由实验得知用电解法将电解液中的金属离子还原为金属单质时,电极所通过的电荷量Q正比于金属的物质的量n和金属离子化合价a的乘积,Q=F·na,其中F是一恒量,称为法拉第常数,它与金属的种类无关(阿伏加德罗常数NA=6.023×1023 mol-1,电子电荷量e=1.6×10-19 C,Cu的摩尔质量:64×10-3 kg·mol-1)。
(1)试求出法拉第常数F(电荷量以库仑为单位,保留三位有效数字)。
(2)如果电解硫酸铜溶液获得1 kg的金属铜,通过电解槽的电荷量是多少?
(3)用电镀的方法在半径为R的铜球表面均匀地镀上很薄的银层,在电镀槽中铜球是阳极还是阴极?另一电极是什么材料?若电流为I,通电时间为t,银的相对原子质量为A,金属银的密度为ρ,求镀层的厚度d。
两个串联的电解池A和B,分别盛有AgNO3溶液和NaCl溶液,用惰性电极进行电解,当B池的阴极上收集到2.24 L(标准状况)气体时,在A池的阳极上析出物质多少克?若两种溶液都是2 L,两池溶液的pH各是多少?