下列实验方案合理的是
| A.除去苯中的少量苯酚:加入浓溴水振荡、静置后过滤,除去三溴苯酚沉淀 |
| B.检验酒精中的少量水:向酒精中加入足量生石灰 |
| C.制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应 |
| D.除去乙烯中杂质气体:将实验室制得的乙烯气体通入NaOH 溶液 |
现有Al、Cl2、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是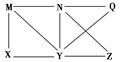
| A.N一定是HCl(aq) | B.X可能为Al或Cl2 |
| C.Y一定为NaOH(aq) | D.Q、Z中的一种必定为Al2O3 |
下列有关物质检验的实验结论正确的是 ( )
| 选项 |
实验操作及现象 |
实验结论 |
| A |
向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 |
该溶液中一定含有SO |
| B |
向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色 |
该溶液中一定含有Fe2+ |
| C |
将某气体通入品红溶液中,品红溶液褪色 |
该气体一定是SO2 |
| D |
将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热后有银镜生成 |
该物质一定属于醛类 |
宁夏的硒砂瓜现今已享誉区内外,西瓜富含硒元素,有延年益寿、抗衰老、抗癌作用,因之得名“硒砂瓜”。二氧化硒(Se)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。在回收过程当中涉及到如下两个化学反应①SeO2+4KI+4HNO3 Se+2I2+4KNO3+2H2O;
Se+2I2+4KNO3+2H2O;
②Se+2H2SO4(浓) 2SO2↑+SeO2+2H2O下列有关叙述正确的是
2SO2↑+SeO2+2H2O下列有关叙述正确的是
| A.SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)> SeO2> I2。 |
| B.①中Se是氧化产物,I2是还原产物 |
| C.反应①中KI是氧化剂,SeO2是还原剂 |
| D.反应①中每有0.6 mol I2生成,转移电子数目为2.4NA |
将11.9 g Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7 g。另取等质量的合金溶于过量稀硝酸中,生成了6.72 L(标准状况下)NO,向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀质量为
| A.22.1 g | B.27.2 g | C.30 g | D.无法确定 |
常温下,将等浓度的FeSO4和(NH4) 2SO4两种浓溶液混合可制得一种晶体,该晶体是分析化学中常用的一种还原剂,其强热分解反应化学方程式:
2(NH4)2Fe(SO4)2·6H2O Fe2O3+2NH3↑+N2↑+4SO2↑+17H2O
Fe2O3+2NH3↑+N2↑+4SO2↑+17H2O
下列说法正确的是( )
| A.该反应中氧化产物是N2、NH3,还原产物是SO2、Fe2O3 |
| B.1 mol摩尔盐强热分解时转移电子的物质的量为8NA |
| C.向摩尔盐溶液中滴入足量浓NaOH溶液,最终可得刺激性气体和白色沉淀 |
| D.常温下,摩尔盐的溶解度比FeSO4、(NH4)2SO4小 |