往含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示。则原溶液中c(Br-)/c(Cl-)的比值约为
| A.V1/(V2-V1) | B.V1/V2 | C.(V2-V1)/V1 | D.V2/V1 |
设NA为阿伏加德罗常数的值,下列说法中正确的是
| A.常温常压下,2.24 L H2O中含有极性共价键的数目为0.2 NA |
| B.0.1 mol·L-1 NH4Cl溶液中含有NH4+的数目小于0.1 NA |
| C.100 mL 12 mol·L-1的浓HNO3与过量Cu反应转移电子的数目为0.6 NA |
| D.标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2 NA |
25℃时,下列各组离子在指定溶液中一定能大量共存的是
| A.使酚酞变红色的溶液:NH4+、Ca2+、NO3-、SO42- |
| B.c(OH-)=1×10-13 mol·L-1的溶液:Na+、K+、ClO-、SO42- |
| C.0.1 mol·L-1 FeCl2溶液:K+、Na+、SO42-、NO3- |
| D.0.1 mol·L-1 KMnO4溶液:Na+、Mg2+、NO3-、SO32- |
用下列实验装置进行相应实验,能达到实验目的的是(夹持装置未画出)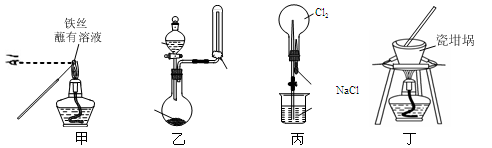
| A.用装置甲检验溶液中是否有K+ |
| B.用装置乙制取并收集少量NH3 |
| C.用装置丙进行喷泉实验 |
| D.用装置丁加热熔融NaOH固体 |
下列有关化学用语表示正确的是
A.过氧化钙(CaO2)的电子式: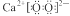 |
B.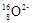 离子的结构示意图: 离子的结构示意图: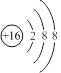 |
C.H2CO3的电离方程式:H2CO3 2H++CO32- 2H++CO32- |
| D.葡萄糖的结构简式:C6H12O6 |
国务院颁布的《“十二五”控制温室气体排放工作方案》提出,2015年我国单位国内生产总值CO2排放要比2010年下降17 %。下列说法不正确的是
| A.CO2属于酸性氧化物 |
| B.CO2是导致酸雨发生的主要原因 |
| C.可用Na2CO3溶液捕捉(吸收)CO2 |
| D.使用氢能源替代化石燃料可减少CO2排放 |