铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)FeCl3溶液用作蚀刻铜箔制造电路板的工艺,离子方程式为
(2)现有一含有FeCl2和FeCl3的混合样品,测得n(Fe): n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为___ _。证明混合物中存在Fe2+的操作: ,在实验室中,FeCl3可用铁粉和___ ____反应制备.
(3)有学生利用FeCl3溶液制取FeCl3·6H2O晶体主要操作包括:滴入过量盐酸, 、冷却结晶、过滤。过滤中要用到的玻璃仪器有漏斗、烧杯和 。
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为___ 。
某二元酸H2A的电离方程式是:H2A=H++HA_, HA_A2_+H+。回答下列问题:
(1)Na2A溶液显(填“酸性”、“碱性”或“中性”),理由是(用离子方程式表示);
(2)NaHA溶液显 (填“酸性”、“碱性”或“中性”),理由是(用离子方程式表示);
(3)若0.1mol·L-1 NaHA溶液的pH=2,则0.1mol·L-1 H2A溶液中氢离子的物质的量浓度可能0.11mol·L-1(填“<”、“>”或“=”),理由是 ;
(4)0.1mol·L-1 NaHA溶液中各离子浓度由大到小的顺序是。
在配制Al2(SO4)3溶液时,铝离子会部分水解而使溶液呈酸性,水解的离子方程式为:。为了防止发生水解,可以加入少量的;在Na2S溶液中,硫离子水解的离子方程是 ;为了防止水解,在配制该溶液时,可以加入少量的 。
若要除去下列各物质中的杂质,写出所用试剂:
(1)除去MgCl2中混有的少量MgCO3,可选用 溶液
溶液
(2)除去FeCl2中混有的少量Cu2+,可选用
(3)除去Fe粉中混有的少量Al粉,可选用 溶液
在金、钠、铁、铝几种金属中,在空气中最稳定的是 、最活泼的是;既能与酸反应又能与碱反应的是;适合于用热还原法冶炼的是。
我校某化学小组欲设计实验检验浓H2SO4和木炭反应的所有产物:
(1)写出浓H2SO4和木炭反应的化学方程式
(2)请你从下图中选用所需的仪器(可重复使用)组成一套装置帮助该小组实现他们的目的.现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)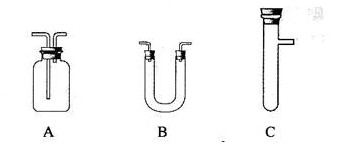
将所选的仪器按连接顺序由上至下依次填入下表(可以不填满,也可以补充),并写出该仪器中应加试剂的名称及其作用。
| 选用的仪器 (填字母) |
加入的试剂 |
作用 |
| (1) (2) (3) (4) (5) · · · |