X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。下列说法不正确的是( )
| A.原子半径:Y>Z>W |
| B.非金属性最强的元素为W |
| C.Y的最高价氧化物对应的水化物为强碱 |
| D.XW2分子中各原子最外层电子均达到8电子结构 |
某混合溶液中只含有两种溶质NaCl和H2SO4,且n(NaCl):n(H2SO4)=3:1。若以石墨电极电解该溶液,下列推断中不正确的是
A.阴极产物为H2 B.阳极先析出Cl2,后析出O2
C.电解液的pH不断增大,最终大于7 D整个电解的过程实质是电解水
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH + 3O2 + 4OH- 2CO32-+ 6H2O,则下列说法错误的是
2CO32-+ 6H2O,则下列说法错误的是
| A.放电时CH3OH参与反应的电极为正极 |
| B.充电时电解质溶液的pH逐渐增大 |
| C.放电时负极的电极反应为:CH3OH-6e-+8OH-= CO32-+ 6H2O |
| D.充电时每生成1 mol CH3OH转移6 mol电子 |
将等质量的a.b两份锌粉装入试管中,分别加入过量的稀硫酸,同时向装a的试管中加入少量CuSO4溶液。下图表示产生氢气的体积V与时间t的关系,其中正确的是
如图两个电解槽中,A.B.C.D均为石墨电极。若电解过程中共有0.02 mol电子通过,下列叙述中正确的是( ) 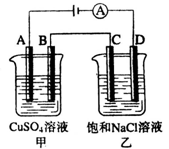
A.甲烧杯中A极上最多可析出铜1.28 g
B.甲烧杯中B极上电极反应式4OH--4e-→2H2O+O2↑
C.乙烧杯中滴入酚酞试液,D极附近先变红
D.烧杯中C极上电极反应式为4H++4e-→2H2↑
某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。放电时的电池反应为:Li+LiMn2O4==Li2Mn2O4。下列说法正确的是
| A.放电时,Li发生还原反应 | B.放电时,正极反应为:Li++LiMn2O4+e-==Li2Mn2O4 |
| C.充电时,LiMn2O4发生氧化反应 | D.充电时,阳极反应为:Li++e-==Li |