化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如下图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( )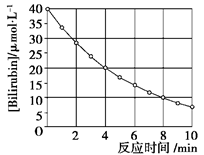
| A.2.5 μmol·L-1·min-1和2.0 μmol·L-1 |
| B.2.5 μmol·L-1·min-1和2.5 μmol·L-1 |
| C.3.0 μmol·L-1·min-1和3.0 μmol·L-1 |
| D.5.0 μmol·L-1·min-1和3.0 μmol·L-1 |
NA代表阿伏加德罗常数,以下说法正确的是()
| A.9g水所含电子数为 5NA |
| B.常温常压下1 mol NO2气体与水在无氧条件下反应生成NA个NO3-离子 |
| C.标准状况下,11.2L三氧化硫溶于水,可生成0.5NA个硫酸分子 |
| D.62 g Na2O溶于水后所得溶液中含有Na+ 离子数为NA |
新型解热镇痛抗炎药扑炎痛的结构如图所示,下列关于扑炎痛的叙述正确的是
| A.该物质的分子式为C17H16NO5 |
| B.该物质的核磁共振氢谱上共有8-个峰 |
| C.该物质与浓溴水反应生成白色沉淀 |
| D.该物质在酸性条件下水解最终可以得到3种物质 |
一定条件下,体积为2L的密闭容器中,1molX和3molY进行反应:
X(g)+3Y(g) 2Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是()
2Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是()
| A.以X浓度变化表示的反应速率为1/8mol/(L·S) |
| B.12s后将容器体积扩大为10L,Z的平衡浓度变为原来的1/5 |
| C.若增大X的浓度,则物质Y的转化率减小 |
| D.若该反应的△H<0 ,升高温度,平衡常数K减小 |
100mL0.1 mol·L-1 NaOH溶液与100mL0.1 mol·L-1 CH3COOH溶液混合后,溶液中离子浓度关系正确的是()
| A.c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| B.c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| C.c(Na+)+ c(OH-)= c(CH3COO-)+ c(H+) |
| D.c(Na+)+ c(H+) = c(CH3COO-)+ c(OH-) |
X、Y、Z是3种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期。X原子的最外层电子数是其电子层数的3倍。Z原子的核外电子数比Y原子多1。下列说法正确的是()
| A.元素X、Y的氢化物沸点Y的较高 |
| B.Z元素最高价氧化物对应水化物的化学式可表示为HYO4 |
| C.Y单质可在X的单质存在时燃烧产生化合物YX3 |
| D.离子半径Z>Y |