下表是实验室制备气体的有关内容:
| 编号 |
实验内容 |
实验原理 |
发生装置 |
| ① |
制氧气 |
  |
|
| ② |
制氨气 |
 |
|
| ③ |
制氯气 |
 |
|
(1)根据表中所列实验原理,从下列装置中选择合适的发生装置,将其编号填入上表的空格中。
(2)上述气体中,从反应中有无电子转移的角度看,明显不同于其他气体的是 ,写出实验室制取该气体的化学方程式 .
(3)若用上述制备 的装置制备
的装置制备 ,应选择的试剂为 .
,应选择的试剂为 .
(4)制备 需用
需用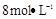 的盐酸1OOml,现用
的盐酸1OOml,现用 的盐酸来配制。
的盐酸来配制。
①需要用量筒量取 的盐酸的体积为 mL;
的盐酸的体积为 mL;
②实验室提供有如下仪器,为完成配制需要选择的仪器为(填序号) 。
A.100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶
E.lOmL量筒 F.胶头滴管 G.lOOmL烧杯 H.lOOmL容量瓶
③下列实验操作中,不正确的是 (填写标号)。
A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加入蒸馏水到距离刻度线1~2cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次
某同学设计如图所示装置分别进行探究实验(夹持装置已略去)
| 实验 |
药品 |
制取气体 |
量气管中的液体 |
| ① |
Cu、稀HNO3 |
NO |
H2O |
| ② |
FeCl3溶液、双氧水 |
H2O |
|
| ③ |
Zn、稀H2SO4 |
H2 |
H2O |
| ④ |
NaOH固体、浓氨水 |
NH3 |
|
| ⑤ |
Na2CO3固体、稀H2SO4 |
CO2 |
|
| ⑥ |
镁铝合金、NaOH溶液(足量) |
H2 |
H2O |
请回答下列问题:
(1)本实验应对量气管多次读数,读数时应注意
①,
②,③视线与凹液面最低处相平。
(2)实验②收集的气体是。
(3)若向实验③反应体系中加少量CuSO4溶液,反应速率加快,原因是。
(4)实验④、⑤中,量气管中的液体分别是、。
| A.稀H2SO4 | B.CCl4 | C.饱和Na2CO3溶液 | D.饱和NaHCO3溶液 |
(5)在25℃,101kPa条件下,取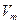 =24.0L/mol。实验⑥数据如下:
=24.0L/mol。实验⑥数据如下:
| 编号 |
镁铝合金质量 |
量气管第一次读数 |
量气管第二次读数 |
| 1 |
1.0g |
20.0mL |
382.2mL |
| 2 |
1.0g |
20.0mL |
360.0mL |
| 3 |
1.0g |
20.0mL |
377.8mL |
根据上述合理数据计算镁铝合金中铝的质量分数。
某化学课外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置。A中所用试剂从下列固物质中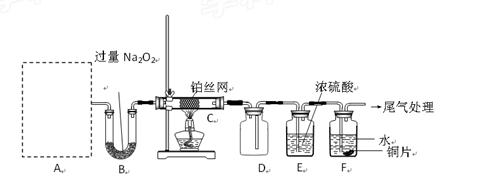
a. NH4HCO3、b. NH4Cl、c. Ca(OH)2、d. NaOH。
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯。部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解。
(1)实验室制取A中气体时若只用一种试剂,该试剂是________(填备选试剂的字母);此时A中主要的玻璃 仪器有________________(填名称)。
仪器有________________(填名称)。
(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:_____________________。
(3)对于C中发生的可逆反应,下列说法正确的是________。
a. 增大一种反应物的浓度可以提高另一种反应物的转化率
b. 工业上进行该反应时,可采取高压的条件提高反应物转化率
c. 该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4∶5
(4)请在下图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式。
(5)待实验结束后,将B中固体混合物溶于500mL1mol·L-1盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是____mol,甲在标准状况下是_____L(忽略气体的溶解)。
某化学课外活动小组进行了一系列“带火星的木条复燃”的实验,实验装置如下图。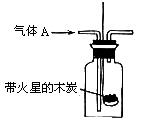
(1)甲组同学探究“使带火星木条复燃时O2的体积分数的极限”。将氧气和空气(假定空气中O2的体积分数为20%)按不同的体积比混合得100mL气体A进行实验,实验记录如下: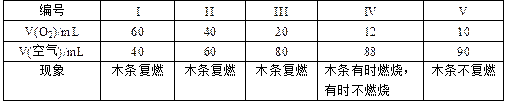
回答问题:
①使带火星木条复燃的O2的体积分数最小(第IV组数据)约为____________。
②用带火星木条检验集气瓶里是否集满O2,若木条复燃,能否认为集气瓶里的气体一定是纯净的O2?答:__________(填“能”或“否”)。
③若按照3:2的比例混合O2和CO2气体,该混合气体能否使带火星的木条复燃?答:___________(填“能”“否”或“不一定”)。
(2)乙组同学探究“NO2能否支持燃烧”的问题,设计了如下几组实验,实验记录及结论如下:
| 编号 |
制取气体A(下列反应产生的混合气体) |
B中的现象 |
结论 |
| a |
在烧瓶中加热适量浓HNO3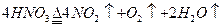 |
充满红棕色气体,木条不复燃,火星熄灭 |
NO2不支持燃烧 |
| b |
加热AgNO3固体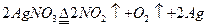 |
充满红棕色气体,木条复燃 |
NO2支持燃烧 |
| c |
加热Cu(NO3)2固体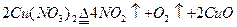 |
充满红棕色气体,木条复燃 |
NO2支持燃烧 |
你认为a、b、c三个结论是否可靠?若不可靠,说明原因;若可靠,则不需说明。
a. ___________,原因是______________________________。
b. ___________,原因是______________________________。
c. ___________,原因是______________________________。
向溴水中加入足量乙醛溶液,可以观察到溴水褪色。对产生该现象的原因有如
下三种猜想:①溴水与乙醛发生了取代反应;②溴水与乙醛发生了加成反应③溴水将乙醛氧化成乙酸。为探究哪一种猜想正确,一研究性学习小组提出了如下两种实验方案:
方案一:检验褪色后溶液的酸碱性
方案二:测定反应前溴水中Br2的物质的量和反应后Br-的物质的量
(1)方案一是否可行?,理由
(2)假设方案二中测得反应前溴水中Br2的物质的量为a mol,若测得反应后n(Br-)=
mol,说明溴水与乙醛发生了取代反应;若测得反应后n(Br-)=mol,说明溴水与乙醛发生了加成反应;若测得反应后n(Br-)=mol,则说明溴水将乙醛氧化成乙酸。
(1)指出在使用下列仪器(已经洗涤干净)或用品时的第一步操作:
①石蕊试纸(检验气体):___________________________________________。
②容量瓶:________________________________________________________。
③托盘天平________________________________________________________。
(2)①现有0.1mol/L的纯碱溶液,请用离子方程式表示纯碱溶液呈碱性的原因:___________________________________________________________________。
②为探究纯碱溶液呈碱性是由CO32-引起的,请你设计一个简单的实验方案:___________________________________________________________________。