如图所示,下列实验操作与方法正确的是:( )
下列叙述正确的是()
| A.一定温度、压强下,气体体积由其分子的大小决定 |
| B.一定温度、压强下,气体体积由其物质的量的多少决定 |
| C.气体摩尔体积是指1 mol任何气体所占的体积为22.4 L |
| D.不同的气体,若体积不等,则它们所含的分子数一定不等 |
用NA代表阿伏加德罗常数的值,下列有关说法正确的是()
| A.78g过氧化钠晶体中,含2NA个阴离子 |
| B.常温常压下,22.4L氦气含有NA个氦原子 |
| C.在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA |
| D.常温下16g O2与O3的混合气体中含氧原子数为NA |
分类方法在化学学科的发展中起到了非常重要的作用。下列分类标准合理的是()
①根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
④根据反应中的热效应将化学化学反应分为放热反应和吸热反应
| A.①② | B.③④ | C.①③ | D.②④ |
20世纪80年代后,人们发现和证实了碳的另一类单质,它们是由一系列偶数个碳原子组成的分子,其中C60(足球烯,分子中含有30个双键)最具代表性。下图所示为n个C60连接而成的物质X。下列有关说法不正确的是()

| A.X难溶于水 | B.一定条件下X可与H2发生加成反应 |
| C.X是碳的一种同素异形体 | D.X的摩尔质量为720n |
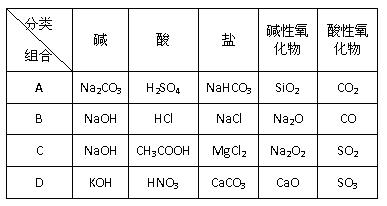
关于物质分类的正确组合()