实验室需配制一种仅含五种离子(水电离出的离子可忽略)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为1 mol/L,下面四个选项中能达到此目的的是
| A.Ca2+、K+、OH−、Cl−、NO3− | B.Fe2+、H+、Br−、NO3−、Cl− |
| C.Na+、K+、SO42−、NO3−、Cl− | D.Al3+、Na+、Cl−、SO42−、NO3− |
对下列化学用语描述和理解都正确的是
A.原子结构示意图 ,可以表示 ,可以表示 ,也表示 ,也表示 |
B.比例模型 可以表示水分子,也可以表示二氧化碳分子 可以表示水分子,也可以表示二氧化碳分子 |
C.结构示意图为 的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 |
D.电子式 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
化学与生活密切相关,下列说法正确的是:
| A.制作航天服的聚酯纤维属于新型无机非金属材料 |
| B.银器久置后表面会变暗,是因为发生了电化学腐蚀 |
| C.Li是最轻的金属也是活动性很强的金属,是制造电池的理想物质 |
| D.海水提取溴、煤的液化、焰色反应都发生了化学变化。 |
如图是四种常见有机物的比例模型示意图。下列说法正确的是 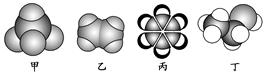
| A.除去甲中混有的少量乙的操作是将混合气体通过盛有酸性KMnO4溶液的洗气瓶。 |
| B.乙和氢气可发生加成反应生成与甲互成同系物的A,A在一定条件下和氯气发生取代反应,最多生成的有机物有六种。 |
| C.丁与丙一样是实验中常用到的萃取剂,并且1mol丁在浓硫酸作用下可与1mol乙酸发生取代反应合成1mol的酯。 |
| D.丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特键,碳原子和氢原子均在同一平面。 |
【原创】水溶液中可能存在Na+、Al3+、Fe2+、NH4+、NO3-、CO32-、SO42-中的基于种离子,且存在的各离子具有相同的物质的量,某同学对该溶液进行如下实验: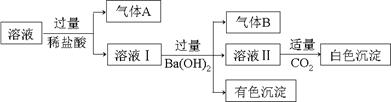
下列判断正确的是
| A.气体A一定是CO2,气体B一定是NH3 |
| B.白色沉淀一定是Al(OH)3 |
| C.溶液中一定存在Al3+、Fe2+、NO3-、NH4+ |
| D.溶液中一定不存在大量Na+ |
25℃时,有c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是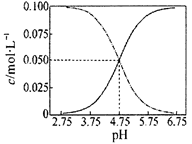
| A.Y点所表示的溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) |
| B.W点所表示的溶液中:c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol·L-1 |
| C.该温度下醋酸的电离平衡常数为0.1 mol·L-1 |
| D.向X点所表示的溶液中加入等体积的0.05 mol·L-1 NaOH溶液 :c(H+)=c(CH3COOH)+c(OH-) |