零排放燃料电池曾被美国《时代》杂志列为21世纪改变人类生活的十大新科技之首。其中最具代表意义的质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极。下列说法中不正确的是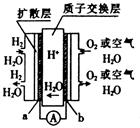
| A.a极为该电池的负极 |
| B.该电池的正极反应式为O2 + 4H+ + 4e-=2H2O |
| C.该电池的能量转化主要形式是化学能转化为电能 |
| D.H+(质子)由正极移动至负极 |
0.1 mol·L-1 AgNO3溶液在以Ag作阳极、Fe作阴极的电解槽中电解,当阴极上增重2.16 g时,下列判断正确的是
| A.溶液的浓度变为0.08 mol·L-1 | B.阳极上产生112 mL O2(标准状况) |
| C.转移的电子数是1.204×1023 | D.反应中有0.02 mol的Ag被氧化 |
单斜硫和正交硫转化为二氧化硫的能量变化如图,下列说法正确的是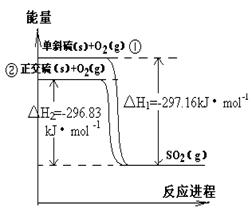
| A.S(s,单斜) = S(s,正交)△H = +0.33kJ·mol -1 |
| B.正交硫比单斜硫稳定 |
| C.相同物质的量的正交硫比单斜硫所含有的能量高 |
| D.①式表示断裂lmol O2中的共价键所吸收的能量比形成1mol SO2中的共价键所放出的能量少297.16kJ |
通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表是一些化学键的键能。
| 化学键 |
C—H |
C—F |
H—F |
F—F |
| 键能/(kJ·mol-1) |
414 |
489 |
565 |
155 |
根据键能数据估算下列反应CH4(g)+4F2(g)===CF4(g)+4HF(g)的反应热ΔH为
A.-1940kJ·mol-1 B.1940kJ·mol-1C.-485kJ·mol-1 D.485kJ·mol-1
爱迪生电池在充电和放电时发生的反应:Fe+NiO2+2H2O 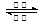 Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是:
Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是:
① 放电时,Fe参与负极反应,NiO2参与正极反应
② 充电时,阴极上的电极反应式为:Fe(OH)2 + 2e-=" Fe" + 2OH-
③ 放电时,电解质溶 液中的阴离子向正极方向移动
④ 放电时,负极上的电极反应式为:Fe + 2H2O-2e- = Fe(OH)2 + 2H+
⑤ 蓄电池的电极必须浸入某种碱性电解质溶液中
| A.只有③ | B.③④ | C.④⑤ | D.①②⑤ |
当电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是
| A.电池的正极反应式为:O2十2H2O十4e-=4OH- |
| B.当电池负极消耗mg气体时,电解池阳极同时有mg气体生成 |
| C.电解后c(Na2CO3)变小 |
| D.电池中c(KOH)不变;电解池中溶液pH变大 |