W、X、Y、Z四种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族。请回答下列问题。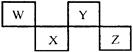
(1)请写出各对应的元素符号:W、 X、 Y、 Z 。
(2)W、Y和氢3种元素所形成的一种化合物,其75%(体积分数)的溶液常用于医疗消毒,该化合物的化学式为
(3)电解NaZ水溶液时,总反应化学方程式为 。工业上,以上述反应的阳极产物和Ca(OH)2为原料,制备漂白粉反应的化学方程式为 。
(4)已知:元素钠与元素Y可组成原子个数比为1:1的化合物。请写出该化合物与含W的最高价氧化物发生反应的化学方程式为 。
(6分)"比较"是化学研究物质性质的基本方法之一,请运用比较法解答下列问题:
已知在一定条件下,过氧化钠几乎可与所有的常见气态非金属氧化物反应。
如:2Na2O2+2CO2=2Na2CO3+O2,Na2O2+CO=Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式。
。
。
(2)当1 mol SO3参加反应时,转移电子的物质的量为mol。
(3)通过比较可知:在气态非金属氧化物中,当非金属元素处于价时,其氧化物与过氧化钠反应就有O2生成。
某河道两旁有甲、乙两厂。它们排放的工业废水中,共含 K+、Ag+、Cu2+、OH-、Cl-和NO3-六种离子。
(1)甲厂的废水明显呈碱性,故甲厂废水中含有的三种离子分别是、、(填离子符号);
(2)乙厂的废水中含有另外三种离子。如果加一定量(选填:活性炭、硫酸亚铁、铁粉),可以回收其中的金属、、(填写金属元素符号)。
(3)另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的、、、(填写离子符号)转化为沉淀。经过滤后的废水主要含(填写化学式),可用作肥料来浇灌农田。
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题: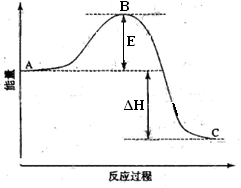
(1)图中A、C分别表示 、 ,E的大小对该反应的反应热 (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点 (填“升高”还是“降低”),△H (填“变大”、“变小”或“不变”),理由是
(2)图中△H= KJ·mol-1
发射卫星用N2H4为燃料,NO2为氧化剂,两者反应生成N2和水蒸气, 已知
N2(g)+2O2(g)=2NO2(g)⊿ H1= + 67.7kJ/mol;
N2H4(g)+O2(g)= N2(g)+2H2O(g)⊿ H2 = - 534kJ/mol;
2H2(g)+ O2(g)= 2H2O(g)⊿ H3= - 484kJ/mol;
H2(g)+F2(g)=2HF(g)⊿ H4= - 538kJ/mol
写出N2H4与 NO2反应的热化学方程式________________________________________,
写出N2H4与F2反应的热化学方程式__________________________________________。
已知H2 ( g ) + 1/2O2 ( g ) = 2H2O ( g ) ,反应过程中能量变化如下图: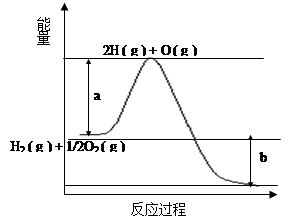
请回答下列问题:
(1)图中a,b分别代表什么意义?
a.;b.。
(2)该反应是反应(填“吸热”或“放热”),△H(填“< 0”或“> 0”)。