同温同压下,若A容器中充满气体Ox和B容器中充满气体Oy
(1)若所含分子总数相等,则A容器和B容器的容积之比是 (用x、y表示,下同)
(2)若两容器中所含原子总数相等,则A容器和B容器的容积比是
(3)若两容器的体积比为y∶x,则Ox和Oy物质的量之比为_________,质量之比为_______,密度之比为______________。
取A、B两份物质的量浓度相等的NaOH溶液,体积均为50mL,分别向其中通入一定量的CO2后,再分别稀释为100mL。
(1)在NaOH溶液中通入一定量的CO2后,溶液中的溶质的组成可能是:
(2)在稀释后的溶液中分别逐滴加入0.1mol·L-1的盐酸,产生的CO2的体积(标准状况)与所加盐酸的体积关系如右图所示: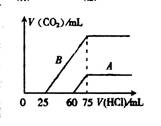
①分别加入足量的盐酸后,溶液中的溶质是,
原NaOH溶液的物质的量浓度是。
②A曲线表明,NaOH溶液通入CO2后,所得溶液中的溶质
是,与盐酸反应产生CO2的最大体积是mL(标准状况)。
③B曲线表明,原NaOH溶液通入CO2后,所得溶质的化学式为,其物质的量之比为。
过碳酸钠(2Na2CO3·3H2O2 )是一种新型高效固体漂白杀菌剂,它具有无臭、无毒、无污染的特点,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中。依托纯碱厂制备过碳酸钠可降低生产成本,其生产流程如下:
)是一种新型高效固体漂白杀菌剂,它具有无臭、无毒、无污染的特点,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中。依托纯碱厂制备过碳酸钠可降低生产成本,其生产流程如下: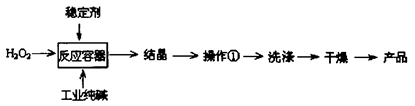
试回答下列问题:
(1)过碳酸钠溶于水后所得溶液一定显(“酸性”、“碱性”或“中性”)。
(2)操作①需要的玻璃仪器有(填写仪器名称)。
(3)工业纯碱中常含有少量NaCl,某校化学课外活动小组 设计如图所示装置,测定工业纯碱中Na2CO3的含量。
设计如图所示装置,测定工业纯碱中Na2CO3的含量。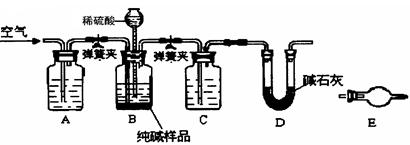
①要检验工业纯碱中杂质的存在,最好选用下列试剂中的(选填序号)。
a.氢氧化钡溶液 b.稀硝酸 c.硫氰 化钾溶液 d.硝酸银溶液
化钾溶液 d.硝酸银溶液
②检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若,说明
装置不漏气。
③装置A的作用是,装置C中的试剂为。
④某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?
(选填“必要”或“不必要”),判断的理由 。
。
已知:①卤代烃可以和某些金属反应生成烃基金属有机化合物 。后者又能与含羰基( )的化合物反应生成醇:
。后者又能与含羰基( )的化合物反应生成醇: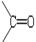
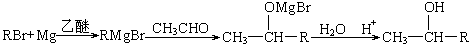
②苯在AlCl3催化下能与酰卤发生如下反应: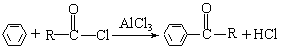
有机物E可由下述路线合成: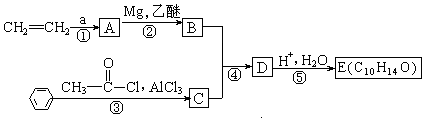
E与硫酸共热到适当温度可得到F和G。F分子中所有碳原子均可共处于同一平面上,G中只含有一个甲基。回答下列问题:
(1)C、D的结构简式分别是:C,D。
(2)G中核磁共振氢谱中氢原子的类型有种。
(3)写出F形成高聚物反应的化学方程式:。
(4)写出下列反应的化学方程式:
①,
④ 。
。
(5)E′是E的同分异构体且与E属同一类别。若E′不能从羰基化合物直接加氢还原得到,则E′可能的结构简式为(有几种写几种,下同);若E′能被催化氧化生 成醛,且E′与浓硫酸共热不能得到碳链不变的烯烃,E′为苯的一取代物,则E′可能的结构简式为。
成醛,且E′与浓硫酸共热不能得到碳链不变的烯烃,E′为苯的一取代物,则E′可能的结构简式为。
现有T、X、Y、Z短周期元素,其中T元素原子M层上有6个电子,X元素原子最外层电子数是次外层电子数的2倍,Y单质为双原子分子,其氢化物水溶液呈碱性,Z元素最高正价是+7价。
(1)元素Y与氢元素形成一种离子YH4+,写出该微粒的电子式 (用元素符号表 示)
示)
(2)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填序号)。
(用元素符号表示),下列表述中能证明这一事实的是 (填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(3)比较等浓度的Na2XO3溶液中c(XO32-)和NaHXO3溶液中c(HXO3-) 大小,
大小,
c(XO32-) c(HXO3-)(填“>” “=”或“<”)
(4)A、J为常见的金属,G为T元素的最高价氧化物对应的水化物,B的溶液呈蓝色。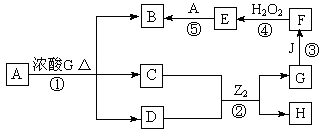
请回答下列问题:
①写出H的化学式____________________;
②写出反应①的化学方程式______________________________;
③写出酸性条件下反应④的离子方程式______________________________。
1 L某混合溶液,可能含有的离子如下表:
| 可能大量含有的阳离子 |
H+NH4+Al3+K+ |
可能大量含有 的阴离子 的阴离子 |
Cl-Br-I‑ClO‑AlO2- |
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(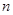 )与加入NaOH溶液的体积(
)与加入NaOH溶液的体积(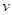 )的关系如右图所示。
)的关系如右图所示。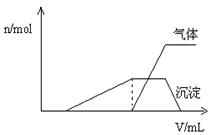
则该溶液中确定含有的离子有____________________;
不能确定是否含有的阳离子有____________________,
要确定其存在可补充做的实验是____________________;
肯定不存 在的阴离子有____________________。
在的阴离子有____________________。
(2)经检测,该溶液中含有大量的Cl— 、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积标准状况)的关系如下表所示,分析后回答下列问题:
| Cl2的体积(标准状况) |
2.8L |
5.6 L |
11.2 L |
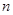 (Cl-) (Cl-) |
1.25mol |
1.5 mol |
2 mol |
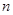 (Br-) (Br-) |
1.5 mol |
1.4 mol |
0.9 mol |
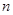 (I-) (I-) |
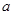 mol mol |
0 |
0 |
①当通入Cl2的体积为2.8 L时,溶液中发生反应的离子方程式为____________________。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为______________________________。