设NA为阿伏伽德罗常数的值。下列叙述正确的是( )
| A.1mol Al3+离子含有的核外电子数为3NA |
| B.25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C.1mol Cl2与足量的铁反应,转移的电子数为3NA |
| D.常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA |
如图,条件一定时,反应2NO(g)+O2(g) 2NO2(g)△H<0中NO2的百分含量NO2%与T变化关系曲线图,图中有a、b、c、d四个点,其中表示未达到平衡状态,且v正<v逆的点是()
2NO2(g)△H<0中NO2的百分含量NO2%与T变化关系曲线图,图中有a、b、c、d四个点,其中表示未达到平衡状态,且v正<v逆的点是()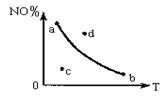
| A.a | B.b | C.c | D.d |
下图各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由快到慢的顺序为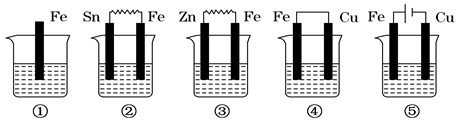
| A.⑤②①③④ | B.④③①②⑤ | C.⑤④②①③ | D.③②④①⑤ |
可逆反应mA(s)+nB(g)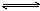 pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图,根据图中曲线分析,判断下列叙述中正确的是
pC(g)+qD(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图,根据图中曲线分析,判断下列叙述中正确的是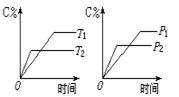
| A.到达平衡后,若使用催化剂,C的质量分数增大 |
| B.平衡后,若升高温度,平衡则向逆反应方向移动 |
| C.平衡后,增大A的量,有利于平衡向正反应方向移动 |
| D.化学方程式中一定n>p+q |
下图是恒温下某化学反应的反应速率随反应时间变化的示意图。下列叙述与示意图
不相符合的是
| A.反应达平衡时,正反应速率和逆反应速率相等 |
| B.该反应达到平衡态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡态Ⅱ |
| C.该反应达到平衡态后,减小反应物浓度,平衡发生移动,达到平衡态Ⅱ |
| D.同一种反应物在平衡态Ⅰ和平衡Ⅱ时浓度不相等 |
某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)  Z(g)+W(s)△H>0下列叙述正确的是
Z(g)+W(s)△H>0下列叙述正确的是
| A.加入少量W,逆反应速率增大 | B.当容器中气体压强不变时,反应达到平衡 |
| C.升高温度,平衡逆向移动 | D.平衡后加入X,上述反应的△H增大 |