25 ℃时,某硫酸铜溶液的质量分数为w,物质的量浓度为c mol·L-1,密度为ρ g·mL-1,将此溶液蒸去a g水或再向原溶液中加入b g无水硫酸铜粉末,充分静置并恢复至25 ℃时,均恰好全部转化为CuSO4·5H2O晶体。则下列关系式正确的是( )
A.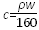 |
B. |
C.16a=9b | D.9a=16b |
分子式为C7H6Cl2属于芳香族化合物的同分异构体有几种
| A.7种 | B.8种 | C.9种 | D.10种 |
下列说法正确的是
A.用氯酸钾固体和浓盐酸制氯气的反应方程式: |
| B.向含有大量Ca2+、Cl—、Al3+的溶液中通入适量SO2,有沉淀生成 |
| C.用少量酸性KMnO4溶液可以检测FeCl3浓溶液中是否含有Fe2+ |
| D.常温下Ksp[Cu(OH)2]=2.2×10-20,则常温下2.2mol/L CuCl2溶液的pH不大于4 |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是
| A.通常情况下,7.6g CS2含有非极性键数目为0.4NA |
| B.22.4L CO气体与1mol N2所含的电子数相等 |
| C.将7.8gNa2O2放入足量的水中,反应时转移0.1NA电子 |
| D.25℃时,1L pH=13的Ba(OH)2溶液中含OH—数目为0.2NA |
下列说法不正确的是
| A.重复使用布袋购物、以步代车等都属于“低碳生活”方式 |
| B.PM2.5指直径小于或等于5μm的“细颗粒物”,该“细颗粒物”属于胶体 |
| C.食品保鲜膜、一次性食品袋的主要成分是聚乙烯 |
| D.用含有橙色的酸性重铬酸钾的仪器检验酒后驾车,利用乙醇的还原性 |
固体X只可能由A1、(NH4)2SO4 ,MgCl2.FeCl2, AlCl3, AgN03中的一种或几种组成,某同学对该固体进行了如下实验
下列判断正确的是:
| A.气体甲一定是纯挣物 |
| B.白色沉淀甲可能是混合物 |
| C.固体X中一定存在AlCl3、(NH4)2SO4, MgCl2 |
| D.固体X中一定不存在FeCl2、AgNO3 |