(14分) (1) 2009年,长春应用化学研究所在甲醇燃料电池技术上获得新突破,原理如下图所示。
①请写出从C口通入O2发生的电极反应式___________________。
②以石墨电极电解饱和食盐水,电解开始后在______________的周围(填“阴极”或“阳极”)先出现红色。假设电池的理论效率为80%(电池的理论效率是指电池产生的最大电能与电池反应所释放的全部能量之比),若消耗6.4g甲醇气体,外电路通过的电子个数为__________________(保留两位有效数字)。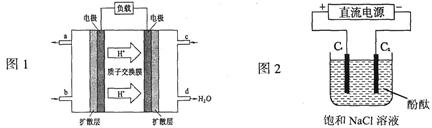
(2)工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,依据沉淀转化的原理,常用FeS等难溶物质作为沉淀剂除去这些离子。已知室温下Ksp(FeS)=6.3×10-18mol2•L-2,Ksp(CuS)=1.3×10-36mol2•L-2。
请用离子方程式说明上述除杂的原理___________________________________________。
(3)工业上为了处理含有Cr2O72-的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
①氧化还原过程的离子方程式为______________________________________________。
②常温下,Cr(OH)3的溶度积Ksp =1×10—32 mol4•L-4,溶液的pH至少为____,才能使Cr3+沉淀完全。
③现用上述方法处理100m3含铬(+6价)78mg•L—1的废水,需用绿矾的质量为 kg。(保留主要计算过程)
将含有C、H、O的有机物3.0g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过装有CaCl2(A)和碱石灰(B)的干燥管,测得A管质量增加了1.8 g,B管质量增加了4.4 g,已知该有机物的相对分子质量为60。(1)燃烧此有机物3.0 g需消耗O2(标准状况)L;(2)求此有机物的分子式。
如下图所示,A、B、C是实验室常用的三种制取气体的装置,提供的药品有:大理石、浓盐酸、稀盐酸、锌粒、二氧化锰、氯化铵、熟石灰。现欲利用这些药品分别制取NH3、Cl2、H2、CO2四种气体,试回答以下问题。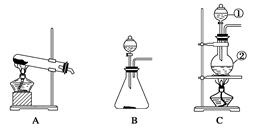
(1)选用A装置可制取的气体有;选用B装置可制取的气体有;通常选用C装置制取的气体有。若用亚硫酸钠和浓硫酸来制取二氧化硫气体应选用装置(填装置的编号字母)。
(2)写出利用上述有关药品制取氯气的化学方程式:。
(3)若要制得干燥的氨气,可选用下列干燥剂中的(填序号)。
A.生石灰 B.浓硫酸 C.五氧化二磷
(4)标号①的仪器除可用于在气体发生装置中添加试剂外,在实验中常用于(填实验操作名称)。
在试管A中加入3mL乙醇,然后边振荡管边慢慢加入2mL浓硫酸和2mL乙酸,按下图所示连接好装置进行实验,以制取乙酸乙酯。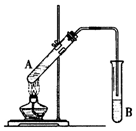
(1)试管B中盛放的试剂是(填名称),实验时往往在B试管中可以看到少量气泡,写出与此现象对应的离子方程式。
(2)乙醇与乙酸反应的化学方程式是。
(3)实验完成后,试管B的液面上有透明的不溶于水的油状液体产生。若要分离B中的液体混合物需要用到的玻璃仪器是。
(4)用30g乙酸与46g乙醇反应,如果实验产率是理论产率的60%,则可得到的产物质量是g。
(5)某同学采用“CH3CH218OH”做该实验,结果含18O原子的产物的结构简式为,乙酸分子的官能团名称为,乙酸在反应中被取代的原子团的电子式为。
已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平):
Cu+2H2SO4(浓)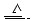 CuSO4+A↑+2H2O
CuSO4+A↑+2H2O
试通过计算和推理完成下面的问题:
(1)A物质可以导致酸雨的形成。则A应该属于(用字母代号填写)
A.酸 B.碱 C.盐D.酸性氧化物 E.碱性氧化物
A物质可以使酸性KMnO4溶液褪色,此反应中(填写化学式,下同)失去电子,氧化剂是。
(2)若A物质通入品红溶液,观察到溶液褪色,说明A物质具有(填序号,下同);若A物质通入Na2S溶液,观察到溶液中出现淡黄色浑浊,说明SO2具有。
A.氧化性 B.还原性 C.漂白性
若A物质通入双氧水,请大胆判断所得溶液是(填溶质的化学式)
(3)一定量的铜片与100mL 18mol/L 的浓H2SO4充分反应,如果该反应过程中转移了0.2mol电子,生成的A气体在标准状况下体积为L (假设气体全部逸出)。若用4 mol·L-1的NaOH溶液吸收生成的A,并生成正盐,写出发生的反应方程式计算需要NaOH溶液的体积L。
A、B、C、D、E是常见化合物或单质,有如下转化关系(略去条件和副产品)。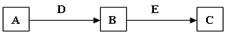
(1)若D为氧气,C为NaAlO2,试写出B转化为C的化学方程式。
(2)若A为气态单质,B为漂白粉的有效成份,C具有漂白性。试写A转化为B的化学方程式。画出组成单质A的元素原子结构示意图。
(3)若A、B、C均为钠盐的水溶液,D、E均为卤素单质,请写出B转化为C的离子方程式。
(4)若A常温下为固态单质,化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,且D、E为同一物质,则B为。
(5)若B、D为质子数小于18的元素原子形成的单质,A、E、C均为氧化物,且D所含元素原子的质子数是B的2倍,A转化为B,B转化为C两个反应均属置换反应,请写出A转化为B的化学方程式。