某混合盐溶液中含有0.2 mol Na+、0.25 mol Mg2+、0.4 mol Cl-和x mol SO42-,则x为
| A.0.1 | B.0.3 | C.0.5 | D.0.15 |
电化学降解法治理水中硝酸盐的污染原理如图所示。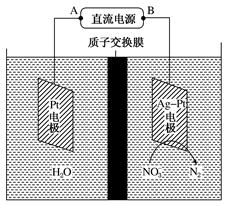
下列说法正确的是
| A.B为电源正极 |
| B.电解过程中H+ 向阳极移动 |
C.阴极反应式为2NO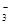 +6H2O+10e-=N2↑+12OH- +6H2O+10e-=N2↑+12OH- |
| D.理论上电解过程中阴、阳两极产生的气体在同温同压下体积比为2︰5 |
下列表示对应化学反应的离子方程式正确的是
| A.NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH- = BaSO4↓+2H2O |
| B.Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH- = CaCO3↓+CO32-+2H2O |
| C.向Ca(ClO)2溶液中通入过量的 SO2:C1O- + SO2 + H2O =" HClO" + HSO3- |
| D.FeSO4酸性溶液中加H2O2:2Fe2++H2O2 = 2Fe3++2OH- |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.0.1molN2与足量的H2反应,转移的电子数是0.6NA |
| B.常温下, 0.1 mol·L-1 NH4NO3溶液中含有的氮原子数是0.2NA |
| C.常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA |
| D.2.24 L CO和CO2的混合气体中所含的碳原子数为0.1 N A |
下图为A、B两种物质间的转化关系(其中C、D是反应物,部分产物已省略)。
以下判断不正确的是
A.若A是AlCl3,则C既可以是强碱,也可以是弱碱
B.若A是碱性气体,则A和C可能发生氧化还原反应,也可能发生非氧化还原反应
C.上述变化过程中,A可以是酸、碱、盐,也可以是单质或氧化物
D.若A→B是氧化还原反应,则C、D在上述转化过程中一定有一种为氧化剂,另一种为还原剂
用下列实验装置进行相应实验,设计正确且能达到实验目的的是 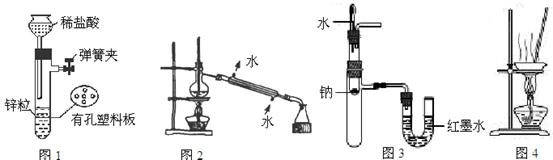
| A.用图1所示装置制取少量H2 |
| B.用图2所示装置分离Na2CO3溶液和CH3COOC2H5的混合物 |
| C.用图3所示装置验证Na和水反应的热效应 |
| D.用图4所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |