X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y 2Z ,一段时间后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率接近于( )
2Z ,一段时间后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则Y的转化率接近于( )
| A.33% | B.40% | C.50% | D.67% |
下列结论可靠的是
A.试液 白色沉淀 白色沉淀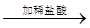 沉淀不溶解 结论:试液中一定含SO42- 沉淀不溶解 结论:试液中一定含SO42- |
B.气体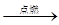 无色气体 无色气体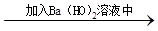 白色沉淀结论:原气体一定是CO 白色沉淀结论:原气体一定是CO |
C.溶液 冒白雾 冒白雾 白烟 白烟结论:原溶液一定是浓盐酸 |
D.有色溶液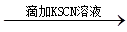 变红色结论:原溶液中一定含Fe3+ 变红色结论:原溶液中一定含Fe3+ |
下列实验现象的描述正确的是
| A.氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白色烟雾 |
| B.氧化铁溶于水生成红褐色沉淀 |
| C.铜在氯气中燃烧,产生棕黄色烟 |
| D.钠在空气中燃烧,发出黄色的火焰,生成白色固体 |
根据世界环保联盟的要求ClO2将逐渐取代Cl2成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,在以上反应中NaClO3和Na2SO3的物质的量之比为 ( )
| A.1︰1 | B.2︰1 | C.1︰2 | D.2︰3 |
能正确表示下列化学反应的离子方程式是 ( )
| A.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| B.硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ |
| C.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O |
| D.向碳酸氢钠溶液中滴加少量稀硝酸:CO32 - + 2H + = CO2 + H2O |
根据反应(1)→(4),可以判断下列4个物质的氧化性由强到弱的正确顺序是()
⑴Cl2+2KI=2KCl+I2;⑵2FeCl2+Cl2=2FeCl3;
⑶2FeCl3+2HI=2FeCl2+2HCl+I2,⑷H2S+I2=S+2HI;
| A.S>I2>Fe3+>Cl2 | B.Cl2>Fe3+>I2>S |
| C.Fe3+>Cl2>S>I2 | D.Cl2>I2>Fe3+>S |