2008年北京奥运会所用火炬燃料为丙烷(C3H8),悉尼奥运会所用火炬燃料为65%丁烷(C4H10)和35%丙烷(C3H8),已知常温下1mol丙烷燃烧放出2220kJ热量,1mol正丁烷燃烧放出2878kJ热量,1mol异丁烷燃烧放出2869.6kJ热量。试回答下列问题:
(1)表示正丁烷燃烧的热化学反应方程式 ;
(2)下列有关说法正确的是 ;
| A.奥运火炬燃烧时的能量转化主要是由化学能转变为热能 |
| B.相同条件下相同质量的正丁烷和丙烷充分燃烧,放出的热量正丁烷的比较多 |
| C.正丁烷比异丁烷不稳定 |
| D.异丁烷分子中的碳氢键比正丁烷的多 |
(3)已知1mol H2燃烧生成液态水放出热量是285.8 kJ,现有5mol 氢气和丙烷的混合气体,完全燃烧时放热3847kJ,则氢气和丙烷的体积比为 。
氮元素是地球大气中含量最多的元素。
(1)氮元素和碳元素一样也存在一系列氢化物并有广泛应用。例如:NH3、N2H4、N3H5、N4H6……。
①写出该系列氢化物的通式:。
②N4H5Cl的同分异构体有种。
(2)NH3、OH-、H2O结合质子(H+)的能力由强到弱的顺序是,其理由用两个反应的离子方程式表示为NH4++OH-= NH3+H2O和。
(3)在碱性介质中,用N2H4与NO2可组合制成燃料电池,产物中无污染物,试写出该电池正极的电极反应式。
(4)①CaCO3和适量稀HNO3溶液反应时,每产生4.4g气体(不考虑气体溶解),放热a kJ,则该反应的热化学方程式为___________________。
②上述反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得pH变化曲线如图所示。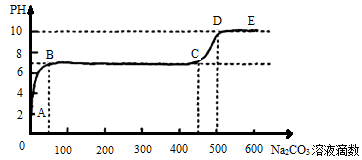
请用离子方程式表示B-C段发生的反应:。
(9分)一定温度下10L密闭容器中发生某可逆反应,其平衡常数表达式为:
根据题意完成下列填空。
(1)写出该反应的化学方程式:;若温度升高,K增大,该反应是(选填“吸热”或“放热”)反应。
(2)下列能判断该反应一定达到平衡状态的是(选填编号)。
a.v正(H2O)=v逆(H2)
b.容器中气体的密度不随时间改变
c.消耗n mol H2同时消耗n mol CO
d.容器中物质的总物质的量不随时间改变
(3)该反应的v正 随时间变化的关系如图。t2时刻改变了某种条件,改变的条件可能是或。
(4)实验测得t2时刻容器内有1molH2O,5min后H2O的物质的量是0.8mol。则这5min内H2O的平均反应速率为。
(8分)硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:H2SO4=H++HSO4-,HSO4- H++SO42-。请回答下列有关问题:
H++SO42-。请回答下列有关问题:
(1)K2SO4溶液呈_______(填“弱酸性”、“中性”或“弱碱性”),其理由是(用离子方程式表示)。
(2)NaHSO4溶液与NaHCO3溶液反应的离子方程式为。
(3)若25℃时,0.10 mol/L的NaHSO4溶液中c(SO42-)="0.03" mol/L,则HSO4-的电离常数Ka=(保留两位有效数字)。0.10 mol/L的H2SO4溶液中c(H+)0.13mol/L (填“>”、“=”或“<”)。
下表是元素周期表一部分,列出了九种元素在周期表中的位置:
| 族 周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
| 2 |
⑤ |
⑥ |
⑦ |
⑧ |
||||
| 3 |
① |
③ |
④ |
⑨ |
||||
| 4 |
② |
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是,在③~⑦元素中,原子半径最大的是;
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是(填物质化学式)。写出①和④的最高价氧化物对应的水化物反应的离子方程式。
(3)用电子式表示③和⑨形成的化合物的形成过程。
(4)表中元素①和⑦可以形成一种淡黄色物质X,写出X的电子式:,该物质所含化学键类型,0.1mol X与水反应转移电子数为:。
(5)表中元素⑥和⑧可形成一种相对分子量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式。
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。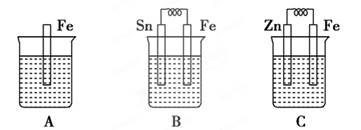
(1)分别写出B、C装置中铁片表面发生的电极反应:
B:________________________________________
C:________________________________________
(2)A、B、C中铁被腐蚀的速率,由快到慢的顺序是_____________
(3)科学工作者为心脏病人设计的心脏起搏器的电池是以Pt和Zn为电极材料,依靠人体内液体中含有一定浓度的溶解氧、H+和Zn2+进行工作。该电池的正极反应:。