某学生用托盘天平称量时,将样品与砝码的位置放颠倒了,待平衡时,称得样品质量为10.5克(1克以下用游码),则样品的实际质量应为( )
| A.9.5g | B.10.0g | C.10.5g | D.11.0g |
一定温度下,在2 L的密闭容器中发生如下反应:A(s)+2B(g) xC(g) △H<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2。
xC(g) △H<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2。
下列有关说法正确的是
A.x=2,反应开始2 min内,v(B)=0.1 mol/(L·min)
B.t1时改变的条件是降温,平衡逆向移动
C.t2时改变的条件可能是增大c(C),平衡时B的物质的量分数增大
D.t3时可能是减小压强,平衡不移动;t4时可能是使用催化剂,c(B)不变
如图所示装置I是一种可充电电池,装置II为电解池。离子交换膜只允许Na 通过,充放电的化学方程式为 2Na2S2+NaBr3
通过,充放电的化学方程式为 2Na2S2+NaBr3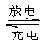 Na2S4+3NaBr。
Na2S4+3NaBr。
闭合开关K时,b极附近先变红色。下列说法正确的是
A.负极反应为4Na 4e 4e =4Na =4Na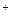 |
B.当有0.01 mol Na 通过离子交换膜时,b电极上析出标准状况下的气体112 mL 通过离子交换膜时,b电极上析出标准状况下的气体112 mL |
| C.闭合K后,b电极附近的pH变小 |
| D.闭合K后,a电极上有气体产生 |
下列溶液中有关物质的量浓度关系正确的是()
A.pH=2的HA溶液与pH=12的MOH溶液任意比混合:
c(H+) + c(M+) ="=" c(OH-) + c(A-)
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:
c(NaOH)<c(CH3COONa)<c(Na2CO3)
C.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-) +2c(OH-) ="=" 2c(H+) + c(CH3COOH)
D.0.1mol·L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
有Wn+、Xm+、Ym-、Zn-四种离子(m>n),且W、X、Y、Z四种原子的M电子层上的电子数均为奇数。下列说法中正确的是
| A.Wn+、Xm+、Ym-、Zn-的离子半径依次增大 |
| B.Y、Z的气态氢化物的热稳定性:YHm>HnZ |
| C.W、X、Y、Z的最高价氧化物对应的水化物都是强电解质 |
| D.W、X、Y、Z的最高价氧化物对应的水化物的碱性依次减弱,酸性依次增强 |
肼(N2H4)是火箭发动机的燃料,反应时N2O4为氧化剂,生成氮气和水蒸气。已知:
N2(g)+2O2(g)=N2O4(g);△H="+8.7kJ/mol"
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534.0kJ/mol
下列表示肼跟N2O4反应的热化学方程式,正确的是()
| A.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-542.7kJ/mol |
| B.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1059.3kJ/mol |
| C.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1076.7kJ/mol |
D.N2H4(g)+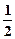 N2O4(g)= N2O4(g)=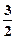 N2(g)+2H2O(g);△H=-1076.7kJ/mol N2(g)+2H2O(g);△H=-1076.7kJ/mol |