. “1.0 mol/L的Na2SO4溶液”的含义是( )
| A.1L水中有1mol Na2SO4 | B.1L溶液中含有142g Na2SO4 |
| C.SO4 2-的物质的量浓度为2.0 mol/L | D.1LNa2SO4溶液中含有Na+1 mol |
NA为阿伏加德罗常数,下列对3mol/L硫酸钾溶液的说法正确的是
| A.1 L溶液中含3NA个K+ |
| B.1 L溶液中含NA个SO42− |
| C.1 L溶液中K+浓度是6 mol•L-1 |
| D.1 L溶液中含6NA个离子 |
在从海带中提取碘的实验中,下列做法错误的是
| A.装有干海带的坩埚置于泥三角上加热灼烧 |
| B.加入过量的氯水确保I-被完全氧化 |
| C.用四氯化碳溶液萃取碘单质,上层为水层可以弃去 |
| D.可利用碘单质易升华的特性来提纯碘单质 |
已知氨气极易溶于水,而难溶于有机溶剂CCl4,下列装置中不适宜做NH3的尾气吸收的是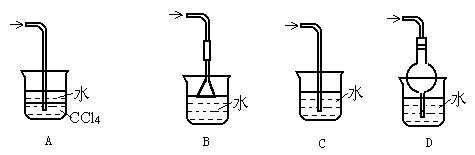
为了除去粗盐中的Ca2+、Mg2+、SO42-可将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量Na2CO3溶液,⑤加过量BaCl2溶液.正确的操作顺序是
| A.①④②⑤③ | B.④①②⑤③ | C.④②⑤①③ | D.⑤②④①③ |
除去下列溶液中的杂质(括号内是杂质)所用试剂正确的是
| A.NaOH溶液(Ba(OH)2):用K2SO4溶液 |
| B.NaCl溶液(Na2SO4):用Ba(NO3)2溶液 |
| C.KOH溶液(K2CO3):用CaCl2溶液 |
| D.HNO3溶液(HCl):用AgNO3溶液 |