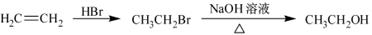黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(1)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g) + O2(g) 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有 (填字母)
| A.升高温度 | B.降低温度 | C.增大压强 | D.减小压强 |
E、加入催化剂 G、移出氧气
(3)SO2尾气用饱和Na2SO3溶液吸收可得到更要的化工原料,反应的化学方程式为 。
(4)将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其原因是 。
已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A。其结构如图: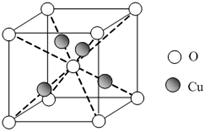
(1)Cu2+电子排布式为 。
(2)元素C、N、O的第一电离能由大到小排列顺序为 。
(3)A中碳原子的轨道杂化类型为 。1mol氨基乙酸钠(H2N-CH2-COONa)含有σ键的数目为 。
(4)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体分子: (写化学式)。
(5)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图,则该化合物的化学式是 。
(14)硫在地壳中主要以硫化物、硫酸盐等形式存在,其单质和化合物在工农业生产中有着重要的应用。
(1)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池的负极的电极反应式 。
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如下图所示。电解时阳极区会产生气体,产生气体的原因是 。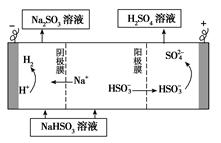
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下: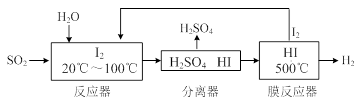
①用离子方程式表示反应器中发生的反应 。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是 。
(3)氢化亚铜是一种红色固体,可由硫酸铜为原理制备
4CuSO4 + 3H3PO2 + 6H2O =" 4CuH↓" + 4H2SO4 + 3H3PO4。
①该反应氧化剂是 (写化学式)。
②该反应每生成1molCuH,转移的电子物质的量为 。
(4)硫酸铜晶体常用来制取波尔多液,加热时可以制备无水硫酸铜,下图是硫酸铜晶体受热分解图示。
请写出A→B的方程式 。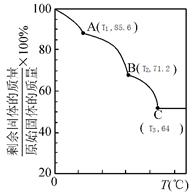
(15分)三氯氧磷(POCl3)无色液体,易水解。用于制取染料中间体,有机合成的氯化剂和催化剂,阻燃剂。还常用作半导体掺杂剂及光导纤维原料。氯化水解法生产三氯氧磷的流程如下:
(1)在反应釜中氯化水解法生产三氯氧磷的化学方程式为 。反应中应控制氯气和水的质量比为3.94,若质量比过小,会导致三氯氧磷产率降低,试分析原因 。
(2)经吸收塔吸收后得到副产品,副产品为(写名称)。
(3)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取a g产品于锥形瓶中,加入足量NaOH溶液,待完全水解后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000 mol·L-1的AgNO3溶液40.00 mL,使Cl-完全沉淀。
Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
Ⅳ.加入指示剂,用c mol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是 (选填字母),滴定终点的现象为 。
a.FeCl2 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②实验过程中加入硝基苯的目的是 ,如无此操作所测Cl元素含量将会 (填“偏大”、“偏小”或“不变”)
(4)氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水,某研究小组想把含磷废水中磷元素转化为磷酸钙沉淀除去,实验操作为 。
可选用的试剂:漂白粉生石灰氯化
| 最佳沉淀pH |
|
| 磷酸氢钙 |
7.0——7.6 |
| 磷酸钙 |
9.0——11 |
摩尔盐[(NH4)aFeb(SO4)c·zH2O]是一种重要化工原料。其组成可通过下列实验测定:
①称取1.5680 g 样品,准确配成100 mL溶液A。
②量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固体0.4660 g。
③再量取25.00 mL溶液A,滴加适量稀硫酸,用0.0200 mol·L-1KMnO4溶液滴定至终点,生成Mn2+,消耗KMnO4溶液10.00 mL。
(1)(NH4)aFeb(SO4)c·zH2O中存在a+2b-2c=0,则该物质中铁元素的化合价为 。
(2)③中发生反应的离子方程式为 。
(3)通过计算确定样品中n(NH4+)∶n(H2O)(必须写出计算过程)。
橙皮素具有抗氧化、消炎、降血脂、保护心血管和抗肿瘤等多种功效。它的合成路线如下: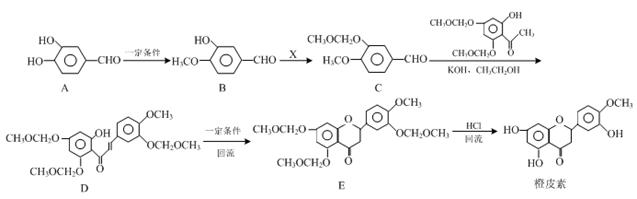
(1)化合物A中的含氧官能团有 、 (填官能团名称)。
(2)已知:B→C为取代反应,其另一产物为HCl,写出X 的结构简式: 。
(3)反应D→E的反应类型是 。
(4)写出同时满足下列条件的B的同分异构体的结构简式: 。
Ⅰ.属于芳香族化合物;
Ⅱ.分子中有4种不同化学环境的氢;
Ⅲ.不能与FeCl3溶液发生显色反应,但能发生水解反应。
(5)已知: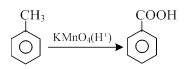
结合流程信息,写出以对甲基苯酚和上述流程中的“X”为原料,制备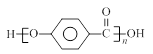 的合成路线流程图(无机试剂任用)。
的合成路线流程图(无机试剂任用)。
合成路线流程图示例如下: