[化学——选修3:物质结构与性质]已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E+原子核外有3层电子且各层均处于全满状态。
请填写下列空白。
(1)E元素基态原子的核外电子排布式为_________________。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为_____________(填元素符号),其原因为_____________________。
(3)B2A4是重要的基本石油化工原料。B2A4分子中B原子轨道的杂化类型为__________;1 mol B2A4分子中含__________molσ键。
(4)已知D、E能形成晶胞如图所示的两种化合物,
化合物的化学式,甲为________,乙为____________;高温时,甲易转化为乙的原因为____________。
已知在容积固定的密闭容器中充入NH3和O2发生如下反应:
4NH3(g)+5O2(g) 4NO(g)+6H2O(g)
4NO(g)+6H2O(g)
(1)下列能说明该反应已经达到平衡状态的是;
A.容器中气体总质量不变
B.c(O2)不变
C.υ(O2)=1.25υ(NH3)
D.体系压强不变
E.相同时间内,消耗0.1 mol NH3,同时消耗了0.1 mol NO
(2)向该容器中加入正催化剂,则反应速率(选填“增大”、“减小”、“不变”,下同),降低容器的温度则反应速率,通入Ar,则反应速率。
(3)若反应在绝热密闭系统中进行时,其余条件不变,反应速率是先增大后减小,其原因是。
A.反应体系温度先升高后降低,所以反应速率是先增大后减小
B.反应物浓度先升高后降低,所以反应速率先增大后减小
C.该反应为放热反应,在反应开始阶段,主要受体系温度升高的影响,反应速率增大;在反应后阶段,主要受浓度减小因素的影响,反应速率减慢
将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:
3A(g)+B(g)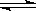 2C(g)+2D(g)
2C(g)+2D(g)
反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol,则:
(1)用C表示10s 内正反应的化学反应速率为;
(2)反应前A的物质的量浓度是;
(3)平衡后,生成物D的浓度为;
乙烯的产量可以用来衡量一个国家的石油化工发展水平。请回答:
(1)若将乙烯气体通入溴的四氯化碳溶液中,反应的化学方程式为:____________________。
(2)可以用来除去乙烷中混有的乙烯的试剂是______。(填序号)
①水②氢气③溴的四氯化碳溶液④酸性高锰酸钾溶液
(3)在一定条件下,乙烯能与水反应生成有机物A.A的结构简式是_____,其反应类型是______反应(填“取代”或“加成”)。
(4)下列化学反应原理相同的是______(填序号)
①乙烯使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色;
②SO2使溴水和酸性高锰酸钾溶液褪色;
③SO2使品红溶液和滴有酚酞的NaOH溶液褪色;
含氮废水进入水体中对环境造成的污染越来越严重。某校环保小组的同学认为可以用金属铝将水中的NO还原成N2,从而消除氮污染。
(1)配平以下有关的离子反应方程式:
□NO3—+□Al+□ H2O―→□ N2↑+□ Al(OH)3+□OH-
(2)以上反应中失电子的物质是________,还原产物是________,每生成1 mol还原产物,将有___个电子发生转移。
(3)现需除去1 m3含氮0.3 mol的废水中的NO(设氮元素都以NO的形式存在),则至少需要消耗金属铝的物质的量为________。
通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是(写出计算过程)。
(2)X与金属钠反应放出氢气,反应的化学方程式是。
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是。
(4)X与酸性高锰酸钾溶液反应可生成Z,在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W。若184 g X和120 g Z反应能生成106 g W,计算该反应的产率(实际产量与理论产量之比)。