化学和环境保护、食品营养、材料应用等密切相关。
(1)防治环境污染,营造安全的生态环境已成为全人类的共识。
①天然水中杂质较多,常需加入明矾、氯化铁等作混凝剂进行处理,混凝剂溶于水后生成的胶体可以吸附水中的悬浮颗粒。请以明矾为例,用离子方程式表示该净水原理 。
②垃圾处理要遵循无害化、减量化和 的原则。
③在汽车尾气系统中装置催化转化器,由于含铅化合物会使 ,所以装有催化转化器的汽车必须使用无铅汽油。
(2)保证食品、药品安全,保持营养均衡,是人体健康的基础。
①人体需要的营养素主要有糖类、油脂、蛋白质、 、维生素和水。在氢、氮、铁、氯、钙这几种元素中,属于人体生命活动必需的微量元素是____________。
②抗酸药物的种类很多,其有效成分一般都是碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝和氢氧化镁等化学物质。某品牌抗酸药的主要成分有糖衣、碳酸镁、淀粉。
写出该抗酸药发挥功效时的离子方程式:________________________________。
③如果不注意控制酸性食物的摄入,就会导致血液偏酸,甚至形成“ 症”,引起人体缺钙、血液黏度增大等。
④阿司匹林是一种人工合成药物,结构简式如右图,常温下与NaOH反应可以得到可溶性钠盐,有比阿司匹林更好的疗效。

请写出此反应的方程式: 。
(3)丰富多彩的材料为人类的生存和发展创造了完美的物质条件。石英玻璃的主要成分为 。有机玻璃受热时会软化,易于加工成型。有机玻璃是一种 (选填“橡胶”或“纤维”或“塑料”)。有些塑料只是在制造过程中受热时能变软,可以塑制成一定的形状,但加工成型后就不会受热熔化,具有 。橡胶是制造轮胎的重要原料,天然橡胶通过硫化处理,使它的分子转化为________结构,从而增大橡胶的强度。
实验室可以用饱和FeCl3溶液制备Fe(OH)3胶体.
(1)写出制备Fe(OH)3胶体的化学方程式
(2)取烧杯中少量Fe(OH)3胶体置于试管中,向试管中滴加稀盐酸至过量,边滴边振荡,可以看到的现象是
周杰伦在歌曲《青花瓷》中唱到“帘外芭蕉惹骤雨,门环惹铜绿”,其中的“铜绿”即是铜锈,它的化学成分是Cu2(OH)2CO3(碱式碳酸铜).铜在潮湿的空气中生锈的化学反应为:2Cu+O2+CO2+H2O═Cu2(OH)2CO3.该反应中的还原剂是 ,清除铜锈可以选择的试剂是 .
(I)在一个容积固定不变的密闭容器中进行反应:2X(g) + Y(g)  2Z(g) ,已知将2molX和1molY充入该容器中,反应在绝热条件下达到平衡时,Z的物质的量为pmol。回答下列问题:
2Z(g) ,已知将2molX和1molY充入该容器中,反应在绝热条件下达到平衡时,Z的物质的量为pmol。回答下列问题:
(1)若把2molX和1molY充入该容器时,处于状态I,达到平衡时处于状态II(如图1),则该反应的△H 0; 熵变△S___ __0 ( 填:“< ,> ,= ”)。该反应在 (填高温或低温)条件下能自发进行。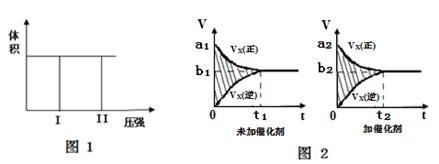
(2)该反应的v-t图像如图2中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,则其v-t图像如图2中右图所示。以下说法正确的是
①a1>a2②b1<b2③t1>t2④右图中阴影部分面积更大⑤两图中阴影部分面积相等
(3)若该反应在容积可变的密闭容器中发生,在温度为T1、T2时,平衡体系中X的体积分数随压强变化曲线如图3所示。下列说法正确的是 。
A.A、C两点的反应速率:A>C
B.A、C两点的气体密度:A<C
C.B、C两点的气体的平均相对分子质量:B<C
D.由状态B到状态A,可以用加热的方法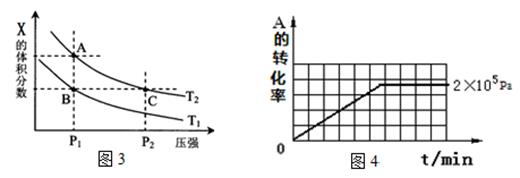
(II)在容积可变的密闭容器中发生反应:mA(g) + nB(g)  pC(g) ,在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表
pC(g) ,在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表
| 压强p/Pa |
2×105 |
5×105 |
1×106 |
| c(A)/mol·L-1 |
0.08 |
0.20 |
0.44 |
(1)当压强从2×105 Pa增加到5×105 Pa时,平衡 移动(填:向左, 向右 ,不)
(2)维持压强为2×105 Pa,当反应达到平衡状态时,体系中共有amol气体,再向体系中加入bmolB,当重新达到平衡时,体系中气体总物质的量是 mol。
(3)其他条件相同时,在上述三个压强下分别发生该反应。2×105 Pa时,A的转化率随时间变化如图4,请在图4中补充画出压强分别为5×105 Pa 和1×106 Pa时,A的转化率随时间的变化曲线(请在图4上画出曲线并标出相应压强)。
有X、Y、Z、R四种短周期主族元素,Y、Z、R同周期。相关信息如下:
| 相关信息 |
|
| X |
单质为双原子分子。若低温蒸发液态空气,因其沸点较低可先获得X的单质 |
| Y |
含Y元素的物质焰色反应为黄色 |
| Z |
同周期元素中原子半径最小 |
| R |
R元素原子的最外层电子数是K层电子数的3倍 |
I.(1)Z元素在周期表的位置是 ,Y、Z、R简单离子的半径从大到小的顺序是 (用离子符号表示);
(2)由X、Z两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子里X、Z两种原子最外层均达到8个电子的稳定结构。甲遇水可形成一种常见的漂白性物质。则甲的结构式为 ;
(3)化合物乙(Y2R)溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Y2R2,其溶液显黄色。则Y2R2的电子式为 ,写出乙溶液在空气中变质生成Y2R2的化学方程式 。
II.元素X与氢可形成多种化合物,如丙、丁、戊。
(4)丙为一元弱酸,酸性与醋酸类似,对热十分稳定但受撞击就爆炸。8.6 g丙爆炸分解生成H2和6.72 L(标况下)X2。写出其爆炸的化学方程式 ;
(5)丁为离子化合物,遇水反应生成H2和气体戊,标况下戊的密度为0.76 g·L-1,则物质丁的化学式为 ;
(6)戊在高温条件下能还原Fe2O3,生成两种单质,写出该反应的化学方程式 ,有人提出生成的产物中可能还有FeO,请设计实验方案验证(用化学方法) 。
在200mLNa2CO3与NaAlO2的混合溶液中逐滴加入1mol·L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+离子的物质的量与加入盐酸溶液的体积变化关系,见下图一所示。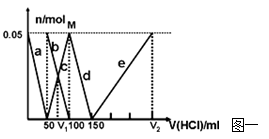
(1)原混合溶液中Na2CO3的物质的量浓度为 mol·L-1
(2)V1: V2= 。
(3)若滴加盐酸过程中得到沉淀0.975g,则滴入盐酸的体积可能为 mL。
(4)在上图二坐标中画出该混合溶液中逐滴加入1mol·L-1的盐酸,所得沉淀的物质的量与加入盐酸溶液的体积变化关系。