(8分)石油通过裂化和裂解可以得到乙烯,乙烯的产量可以用来衡量一个国家石油化工发展水平。下图是由乙烯为原料生产某些化工产品的转化关系图。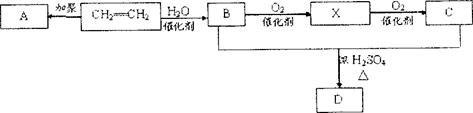
据此回答下列问题。
(1)写出乙烯的一种用途 ,指出乙烯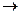 B的反应类型 。
B的反应类型 。
(2)写出A的结构简式 。
(3)写出X和新制的氢氧化铜悬浊液反应的化学方程式 。
(4)写出B+C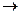 D的化学反应方程式 。
D的化学反应方程式 。
(16分)中国环境监测总站数据显示,颗粒物(PM2.5等)为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1) 将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 |
K+ |
Na+ |
NH |
SO |
NO |
Cl- |
| 浓度/mol•L-1 |
4×10-6 |
6×10-6 |
2×10-5 |
4×10-5 |
3×10-5 |
2×10-5 |
根据表中数据计算PM2.5待测试样的pH =。
(2)NOx是汽车尾气的主要污染物之一。汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
①N2(g)+O2(g) 2NO(g)△H=。
2NO(g)△H=。
②当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式。
(3) 碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:
①用离子方程式表示反应器中发生的反应。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是_____________________。
③用吸收H2后的稀土储氢合金作为电池负极材料(用MH)表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量、长寿命的镍氢电池。电池充放电时的总反应为:Ni(OH)2+M NiO(OH)+MH,电池放电时,负极电极反应式为; 充电完成时,全部转化为NiO(OH),若继续充电,将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸,此时,阴极电极反应式为。
NiO(OH)+MH,电池放电时,负极电极反应式为; 充电完成时,全部转化为NiO(OH),若继续充电,将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸,此时,阴极电极反应式为。
某研究性学习小组探究在含有盐酸的Cu2+、Ca2+的混合溶液中滴加Na2CO3溶液时,发生反应的过程。【已知Ksp{CuOH2}小于Ksp(CuCO3)】
取适量样品溶液,插入pH传感器并逐滴滴入碳酸钠溶液。测得pH变化曲线如下图所示:
(1)为精确控制加入碳酸钠溶液的体积,可将碳酸钠溶液置于(填仪器名称)中滴加。
(2)图中有两个pH增加较快的阶段,第一阶段(a点前)对应的实验现象是。
(3)对于a、b之间溶液的pH值变化缓慢的本质,该小组同学做出了如下推测,请补充推测2和3:
推测1:生成了Cu(OH)2沉淀,消耗了CO32-;
推测2:。
推测3:。
若推测1符合实际情况,则此情况下反应的离子方程式为。
(4)请设计实验验证检验推测1(可不填满),不要写出详细的实验过程,试剂不受限制。
| 实验方法、步骤 |
实验现象和结论 |
研究表明,心形合成药物M在抗非小细胞肺癌方面具有良好的疗效,下面是一种合成M的方法:
已知: I.有机物A的化学式为C7H8O,通过FeCl3溶液有显色反应,其核磁共振氢谱显示有4组吸收峰;
II.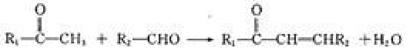
请回答下列问题:
(1)写出E物质的结构简式:。
(2)写出A→B的化学反应方程式:。
步骤①在合成过程中的作用是
(3)E的同分异构体有多种,写出符合下列要求的2中同分异构体的结构简式:
;
a.遇F溶液不显紫色
b.能与NaHCO3反应产生CO2气体
c.苯环上一氧取代产物仅有两种
现有如图所示的转化关系,图中各物质均为常见物质,转化中有部分物质已省略。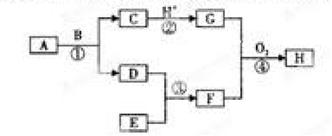
上述物质中C是一种黑色磁性固体,F是极易溶于水且水溶液呈碱性的气体,H是红褐色沉淀,A、D、E均为单质,请回答下列问题:
(1)写出下列物质的化学式:A:、E
(2)写出④中生成H的非氧化还原反应的离子方程式:
(3)在120℃、1大气压下将168gA和90gB放入1L,密封烧瓶中发生反应①,经过10min达到平衡,平衡后D的质量为4g(固体体积忽略不计),则用D表示10min内的平均反应速率为,该温度下此反应的平衡常数K=,B的转化率是。
(1)在常温下,0.5mol甲醇在氧气中完全燃烧生成CO2和液态水,放出热量363.3kJ.写出该反应的热化学方程式: _________________________
(2)请设计一个燃料电池:电解质为强碱溶液,Pt作电极,在电极上分别通入甲醇和氧气。通入甲醇的电极应为极(填“正”或“负”),该电极上发生的电极反应式为。
(3)用Pt电极电解盛有1L pH=6的硝酸银溶液,如图甲所示,则右边电极上发生的电极反应式为 .
(4)某化学学习兴趣小组为了研究金属的腐蚀现象,将一枚铁钉放在“84”消毒液(NaClO)中,某同学设计了如图乙所示实验装置,写出石墨极上发生的电极反应式: