根据下面的反应路线及所给信息填空:
(1)A的结构简式是 ,名称是
(2)①的反应类型 ②的反应类型
(3)反应④的化学方程式
(6分)现有1—20号元素A、B、C、D所对应的物质的性质或微粒结构如下:
①A的原子,M层上有6个电子。②B的离子与D的离子具有相同电子层结构,且可以相互组合形成常见干燥剂。③元素C,常温下单质为双原子分子,其氢化物水溶液呈碱性④元素D,最高正价为+7价。请回答下列问题
(1)B的离子与D的离子相互组合形成的干燥剂的化学式是。
(2)元素C与氢元素形成带一个单位正电荷的离子,写出该微粒的电子式(用元素符号表示)。
(3)元素A与元素D相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是。
a.常温下A的单质和D的单质状态不同 b.A的氢化物比D的氢化物稳定
c.一定条件下D单质能从A的氢化物水溶液中置换出A单质
d.HD的酸性比HA酸性强
C的氢化物固态时属于晶体,该氢化物与A的最高价氧化物水化物反应的化学方程式是。
A~H等8种物质存在如下转化关系(反应条件、部分产物未标出)。已知A是正盐,B是能使品红溶液褪色的气体,G是红棕色气体。按要求回答问题: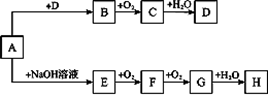
(1)写出下列物质的化学式:A,B。
(2)写出下列反应的化学方程式:E→F;
写出下列反应的离子方程式:A→E;
H的浓溶液与木炭反应的化学方程式:。
(3)检验某溶液中是否含D中阴离子的方法是。
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白: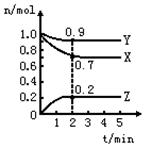
(1)该反应的化学方程式。
(2)反应开始至2min,以气体Z表示的平均反应速率为。
(3)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的倍;
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时_______(填“增大”“减小”或“相等”)。
(8分)下表是元素周期表的短周期部分,表中字母分别表示一种元素。请回答下列问题:
| a |
|||||||
| b |
c |
d |
|||||
| e |
f |
g |
(1) f元素在周期表中的位置是第周期第族。
(2) e 与f两元素最高价氧化物的水化物相互反应的化学方程式为
_____________________________________________________
(3)e在空气中燃烧的产物所含化学键的类型为__________、__________。
(4) 化合物ca3的电子式为,c和d两种元素氢化物的稳定性更强的是 _______(填物质的化学式)。
已知反应:3NO2+H2O==2HNO3+NO,回答下列问题:
(1)该反应的离子方程式为。
(2)氧化剂与还原剂的质量比为,氧化产物与还原产物的物质的量之比为。
(3)在标准状况下,3.36L NO2与H2O完全反应转移的电子数目为。
(4)写出HNO3与石灰水反应的离子方程式。