如图是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图。甲醇在催化剂作用下提供质子(H+)和电子,电子经过电路、质子经内电路到达另一极与氧气反应,该电池总反应式为:2CH3OH+3O2===2CO2+4H2O。下列有关该电池的说法错误的是( )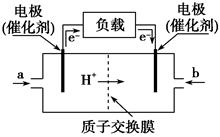
| A.右边的电极为电池的负极,b处通入的是空气 |
| B.左边的电极为电池的负极,a处通入的是甲醇 |
| C.电池负极的反应式为:2CH3OH+2H2O-12e-===2CO2↑+12H+ |
| D.电池正极的反应式为:3O2+12H++12e-===6H2O |
下列说法正确的是
| A.向AgCl悬浊液中加入少量NaCl固体后振荡,c(Cl-)增大,KsP (AgCl)增大 |
B.某溶液中由水电离出的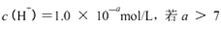 时,则该溶液的pH一定为14-a 时,则该溶液的pH一定为14-a |
| C.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后溶液的pH等于7,则混合溶液 中: 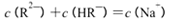 |
D.相同物质的量浓度的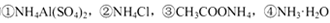 溶液中,c (NH4+)由大到小的顺序是:①>②>③>④ 溶液中,c (NH4+)由大到小的顺序是:①>②>③>④ |
生物燃料电池是以有机物为燃料,直接或简介利用酶作为催化剂的一类特殊的燃料电池,其能量转化效率高,是一种真正意义上的绿色电池。其工作原理如图所示。下列有关说法正确的是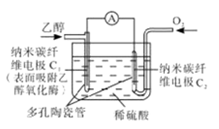
| A.O2在C2电极上得电子,被氧化 |
| B.电子由C2极经外电路流向C1极 |
| C.每转移6mole-,理论上生成22.4LCO2 |
| D.C1极的电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+ |
在盛有足量M的体积可变的密闭容器中加入N,发生反应:M (s) +2N (g)==4P (s) +Q (g) ΔH< 0。在一定温度、压强下达到平衡,平衡时P的物质的量与起始时加入N的物质的量的变化关系如图所示。下列说法正确的是
| A.平衡是N的转化率为50% |
| B.当温度升高后,则图中θ>450 |
| C.若再加入N,则正、逆反应速率均逐渐增大 |
| D.若再加入N,则反应体系中气体密度减小 |
已知X,Y声是元素周期表中前20号元素:|x-y|="3," X, Y能形成化合物M,下列说法正
确的是
| A.若X和Y处于同一周期,则X的原子半径肯定小于Y的原子半径 |
| B.若X和Y处于不同的周期,则M溶于水所得溶液肯定呈碱性 |
| C.若M属于共价化合物,则该分子中原子个数比可能为1:2 |
| D.若M属于离子化合物,则该化合物中只存在离子键 |
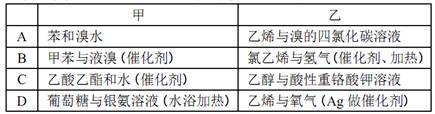
下列各组物质能够发生化学反应,且甲为取代反应、乙为加成反应的一组是