下列离子方程式正确的是( )
①氯气与水反应:Cl2+H2O===2H++Cl-+ClO-
②氯气与氢氧化钠溶液反应:Cl2+2OH-===Cl-+ClO-+H2O
③浓盐酸与二氧化锰共热:MnO2+4HCl Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
④漂白粉溶液中通入少量的二氧化碳气体:Ca2++2ClO-+H2O+CO2===CaCO3↓+2HClO
| A.①③ | B.②④ | C.②③ | D.①④ |
工业上将氨气和空气的混合气体通过铂—铑合金网发生氨氧化反应,若在标准状况下V L氨气完全反应,并转移n个电子,则阿伏加德罗常数(NA)可表示为( )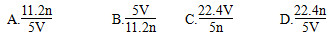
如图是氨气与氯化氢反应的装置。抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)( )
| A.气体反应物的总体积为0.224 L |
| B.生成物的分子个数为0.005NA |
| C.生成物中的N—H键个数为0.02NA |
| D.加水溶解后所得溶液中NH4+数目为0.005NA |
下列叙述正确的是( )
| A.含1 mol溶质的任何溶液,物质的量浓度一定相等 |
| B.配制1 mol·L-1NaCl溶液1 L,其方法是:将58.5 g NaCl溶于1 L水中 |
| C.体积相同、物质的量浓度相同的同种溶液所含溶质的粒子数一定相同 |
| D.1 L 0.5 mol·L-1 CaCl2溶液中,Ca2+与Cl-的物质的量浓度都是0.5 mol·L-1 |
一定温度和压强下,30 L某种气态纯净物中含有6.02×1023个分子,这些分子由1.204×1024个原子组成,下列有关说法中不正确的是( )
| A.该温度和压强可能是标准状况 |
| B.标准状况下该纯净物若为气态,其体积约是22.4 L |
| C.该气体中每个分子含有2个原子 |
| D.若O2在该条件下为气态,则1 mol O2在该条件下的体积也为30 L |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A.常温常压下,8 g O2含有4nA个电子 |
| B.1 L 0.1 mol·L-1的氨水中有nA个NH4+ |
| C.标准状况下,22.4 L盐酸含有nA个HCl分子 |
| D.1 mol Na被完全氧化生成Na2O2,失去2nA个电子 |