下列离子方程式正确的是
| A.碳酸钡与盐酸反应 2H+ + BaCO3= Ba2+ + H2O + CO2↑ |
| B.氢氧化钡溶液与稀硫酸混合 Ba2+ + SO42- + H++ OH-= BaSO4↓+ H2O |
| C.氯气通入蒸馏水中 Cl2 + H2O= Cl- + ClO-+2 H+ |
| D.CO2通入过量的澄清石灰水中 CO2 + Ca(OH)2 = CaCO3↓+ H2O |
下列有关热化学方程式的表示及说法正确的是( )
| A.已知2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol |
| B.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定 |
| C.含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+1/2H2SO4 (aq)=NaCl(aq)+H2O(l) △H=-57.4kJ/mol |
| D.已知I2(g)+ H2(g)=2HI(g) △H1, I2(s)+ H2(g)=2HI(g ) △H2 则△H1>△H2 |
有一处于平衡状态的反应:X(s)+3Y(g) 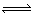 2Z(g),ΔH<0。为了使平衡向生成Z 的方向移动,应选择的条件是()
2Z(g),ΔH<0。为了使平衡向生成Z 的方向移动,应选择的条件是()
①高温 ②低温 ③高压 ④低压⑤加正催化剂⑥分离出Z
| A.①③⑤ | B.②③⑤ | C.②③⑥ | D.②④⑥ |
对于反应2SO2+O2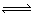 2SO3,下列变化可增大活化分子百分数而使反应速率加快的是( )
2SO3,下列变化可增大活化分子百分数而使反应速率加快的是( )
①增大压强 ②升高温度 ③增大O2浓度 ④使用催化剂
| A.①③ | B.①④ | C.②③ | D.②④ |
一定温度下在容积恒定的密闭容器中,进行反应A(s)+2B(g) 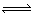 C(g)+D(g),当下列物理量不发生变化时,能说明该反应已达到平衡状态的是( )
C(g)+D(g),当下列物理量不发生变化时,能说明该反应已达到平衡状态的是( )
①混合气体的密度 ②容器内气体的压强 ③混合气体总物质的量 ④B物质的量浓度
| A.①④ | B.只有②③ | C.②③④ | D.只有④ |
下列各组热化学方程式中,化学反应的△H前者大于后者的是()
①C(s)+O2(g) CO2(g); △H1 C(s)+1/2O2(g)
CO2(g); △H1 C(s)+1/2O2(g) CO(g); △H2
CO(g); △H2
②S(s)+O2(g)  SO2(g); △H3 S(g)+O2(g)
SO2(g); △H3 S(g)+O2(g)  SO2(g); △H4
SO2(g); △H4
③H2(g)+1/2O2(g) H2O(l); △H5 2H2(g)+O2(g)
H2O(l); △H5 2H2(g)+O2(g) 2H2O(l); △H6
2H2O(l); △H6
④CaCO3(s) CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)
CaO(s)+CO2(g);△H7 CaO(s)+H2O(l) Ca(OH)2(s);△H8
Ca(OH)2(s);△H8
| A.① | B.④ | C.②③④ | D.①②③ |