ClO2遇浓盐酸会生成Cl2 ,反应方程式为2ClO2 + 8HCl = 5Cl2 + 4H2O ,该反应中若转移电子的数目为9.632×1023,则产生的Cl2在标况下的体积为
| A.11.2L | B.33.6L | C.22.4L | D.44.8L |
下列说法中,正确的是
| A.原子晶体的熔点一定高于离子晶体的熔点 |
| B.第三周期主族非金属元素的氧化物对应的水化物的酸性,从左到右逐渐增强 |
| C.-OH与OH-是不同的微粒,电子式和稳定性各不相同 |
| D.蛋白质、油脂、淀粉等都是人类的重要营养物质,它们都是天然高分子化合物 |
下列有关工业生产的叙述正确的是
| A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 |
| C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
| D.传统的硅酸盐工业为人类提供了大量的建筑等材料。 |
在一定条件下,固定容积的密闭容器中的反应:2NO2(g) O2(g)+2NO(g);ΔH>0,达到平衡时,若改变其中一个条件X,Y随X的变化符合图中曲线的是
O2(g)+2NO(g);ΔH>0,达到平衡时,若改变其中一个条件X,Y随X的变化符合图中曲线的是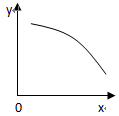
| A.当X表示温度时,Y表示NO2的物质的量 |
| B.当X表示压强时,Y表示NO的转化率 |
| C.当X表示反应时间时,Y表示混合气体的密度 |
| D.当X表示NO2的物质的量时,Y表示O2的物质的量 |
NA为阿伏加德罗常数,下列说法中正确的是
| A.2.24LCl2中的Cl2分子数为0.1 NA |
| B.2.8g乙烯(C2H4)和环丙烷(C3H6)的混合气体中含H原子数为0.5 NA |
| C.C60和C70的混合物共2.4 g,其中所含碳原子数为0.2 NA |
| D.含0.1 mol H2O2的水溶液跟MnO2充分作用,反应过程中转移的电子总数为0.2NA |
下列说法中,正确的是
| A.KW随溶液温度、浓度的改变而改变 |
| B.凡是氧化还原反应,都是放热反应 |
| C.对已达到化学平衡的反应,改变压强,平衡一定改变 |
| D.弱电解质的电离程度,与温度、浓度均有关系 |