在T℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·cm-3,溶质的质量分数为w,其中含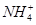 的物质的量为b mol。下列叙述中正确的是( )
的物质的量为b mol。下列叙述中正确的是( )
A.溶质的质量分数为w= ×100% ×100% |
| B.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w |
C.溶液中c(OH-)=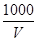 mol·L-1 mol·L-1 |
D.溶质的物质的量浓度c= mol·L-1 mol·L-1 |
下列有关实验装置进行的相应实验,能达到实验目的的是
| A.用图1所示装置除去Cl2中含有的少量HCl |
| B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
| C.用图3所示装置制取少量纯净的CO2气体 |
| D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
能正确表示下列反应的离子方程式是
| A.Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+Ca2++OH-===CaCO3↓+H2O |
| B.等物质的量的MgCl2、Ba(OH)2和HC1溶液混合:Mg2++2OH-= Mg(OH)2↓ |
| C.铜溶于稀硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| D.FeBr2溶液中通入少量的C12:2Fe2++C12= 2Fe3++2C1- |
若用NA表示阿伏加德罗常数的值,下列叙述不正确的是
| A.在0.1 mol NaHSO4晶体中阳离子与阴离子总数为0.2NA |
| B.l L 0.1mol·L-1的H2SO3溶液中含有H+的数目为0.2NA |
| C.7.8 g Na2O2中含有的阴离子数目为0.1NA |
| D.常温常压下,14 g乙烯和丙烯的混合气体中氢原子数为2NA |
向含有c(FeCl3)="0.2" mol·L-l、c(FeCl2)="0.1" mol·L-l的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其中分散质粒子是直径约为9.3 nm的金属氧化物,下列有关说法中正确的是
| A.该分散系的分散质为Fe2O3 |
| B.在电场作用下,阴极附近分散系黑色变深,则说明该分散系带正电荷 |
| C.加入NaOH时发生的反应可能为:Fe2++2Fe3++8OH-=== Fe3O4+4H2O |
| D.可用过滤的方法将黑色金属氧化物与Na+分离开 |
下列分子或离子在指定的分散系中能大量共存的一组是
| A.硝酸钠溶液:H+、Fe3+、SO42-、CH3COOH |
| B.烧碱溶液:K+、HSO3-、NO3-、NH3·H2O |
| C.空气:HCl、CO2、SO2、NO |
| D.氢氧化铁胶体:H+、K+、S2-、Br- |