能正确表示下列反应的离子方程式是
| A.Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+Ca2++OH-===CaCO3↓+H2O |
| B.等物质的量的MgCl2、Ba(OH)2和HC1溶液混合:Mg2++2OH-= Mg(OH)2↓ |
| C.铜溶于稀硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| D.FeBr2溶液中通入少量的C12:2Fe2++C12= 2Fe3++2C1- |
用下图所示装置及药品进行相应实验,能达到实验目的的是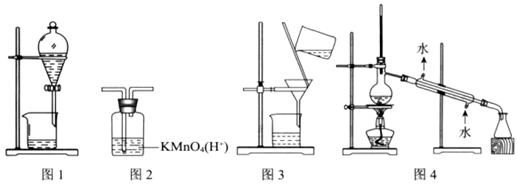
| A.图1分离乙醇和乙酸 | B.图2除去乙炔中的乙烯 |
| C.图3除去溴苯中的溴单质 | D.图4除去工业酒精中的甲醇 |
下列化学方程式不正确的是
A.乙醇与浓氢溴酸反应 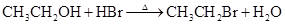 |
B.溴乙烷与氢氧化钠溶液共热 |
C.苯酚钠中通入二氧化碳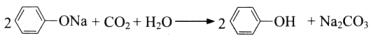 |
D.蔗糖在稀硫酸作用下水解 |
下列醇类物质中,能被氧化成醛的是
下列实验操作不正确的是
| A.实验室制乙烯时,为防止暴沸,应加入沸石 |
| B.不慎将苯酚溶液沾到皮肤上,应立即用稀NaOH溶液清洗 |
| C.饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率 |
| D.向AgNO3溶液中逐滴加入稀氨水,至沉淀恰好溶解,制得银氨溶液 |
下列说法中,正确的是
| A.蛋白质遇硫酸钠溶液变性 | B.天然气的主要成分是甲烷 |
| C.涤纶、锦纶、蚕丝都属于合成纤维 | D.植物油不能使溴的四氯化碳溶液褪色 |