某温度下,密闭容器中发生反应 a X (g)  b Y (g) + c Z (g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是
b Y (g) + c Z (g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是
| A.可逆反应的化学计量数:a>b+c | B.压缩容器的容积时,υ正增大,υ逆减小 |
| C.达到新平衡时,物质X的转化率减小 | D.达到新平衡时,混合物中Z的质量分数增大 |
下列用品所对应的有效成分和用途有错误的是( )
| A |
B |
C |
D |
|
| 用品 |
食盐 |
小苏打 |
明矾 |
漂白粉 |
| 有效成分 |
NaCl |
NaHCO3 |
KAl(SO4)2•12H2O |
CaCl2 |
| 用途 |
做调味品 |
做发酵粉 |
做净水剂 |
做消毒剂 |
环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关物质引起的。下列环境问题与所对应的物质不相关的是()
| A.温室效应——CO2 | B.臭氧层破坏——CO |
| C.酸雨——SO2 | D.光化学污染——NOx |
下列说法正确的是
| A.润洗酸式滴定管时应从滴定管上口加入3~5mL所要盛装的酸溶液,倾斜着转动滴定管,使液体润湿其内壁,再从上口倒出,重复2~3次 |
B.用惰性电极电解MgCl2溶液的离子方程式为:2Cl-+ 2H2O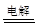 Cl2↑+ H2↑+ 2OH- Cl2↑+ H2↑+ 2OH- |
| C.为验证盐桥的作用,在两个烧杯中分别盛适量硫酸亚铁铵溶液和稀酸性高锰酸钾溶液,分别插入石墨棒用导线与电流计相连,然后用装有K2SO4饱和溶液的琼脂的U型管两端插入两个烧杯中,电流计偏转,一段时间后高锰酸钾溶液褪色 |
| D.嫦娥三号月球车玉兔号在进入第二个月夜休眠前,出现了机构控制异常情况,其病因或为月尘,即月球上直径小于10微米的浮尘,月尘分散在空气中形成的分散系属于胶体。 |
下表是在相同温度下三种酸的一些数据,下列判断正确的是()
| 酸 |
HX |
HY |
HZ |
||
| 浓度(mol/L) |
0.12 |
0.2 |
0.9 |
1 |
1 |
| 电离度 |
0.25 |
0.2 |
0.1 |
0.3 |
0.5 |
| 电离常数 |
Ki1 |
Ki2 |
Ki3 |
Ki4 |
Ki5 |
已知:
A.在相同温度下,从HX的数据可以说明:弱电解质溶液,浓度越低,电离度越大,且Ki1>Ki2>Ki3=0.01
B.室温时,若在NaZ溶液中加水,则c(Z-)/ [c(HZ)• c(OH-)]的比值变小,若加少量盐酸,则比值变大
C.等物质的量的NaX、NaY和NaZ的混合溶液:c(X-)+c(Y-)—2c(Z-)=2c(HZ)—c(HX)—c(HY),且c(Z-)<c(Y-)<c(X-)
D.在相同温度下,Ki5>Ki4>Ki3
用试纸检验气体性质是一种重要的实验方法。如图所示的实验中(可加热),下列试纸的选用、现象、对应结论都正确的一项是( )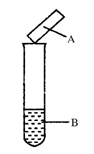
| 选项 |
试剂B |
湿润的试纸A |
现象 |
结论 |
| A |
新制氯水 |
PH试纸 |
变白 |
氯气具有漂白性 |
| B |
浓氨水,生石灰 |
蓝色石蕊试纸 |
变红 |
氨气显碱性 |
| C |
Na2SO3,硫酸 |
品红试纸 |
褪色 |
SO2具有漂白性 |
| D |
Cu,浓硝酸 |
KI淀粉试纸 |
变蓝 |
NO2为酸性气体 |