Q、R、X、Y、Z五种元素的原子序数依次递增。已知: ①Z的原子序数为29,其余的均为短周期主族元素;
①Z的原子序数为29,其余的均为短周期主族元素; ②Y原子价电子(外围电子)排布msnmpn
②Y原子价电子(外围电子)排布msnmpn  ③R原子核外L层电子数为奇数;
③R原子核外L层电子数为奇数; ④Q、X原子p轨道的电子数分别为2和4。
④Q、X原子p轨道的电子数分别为2和4。 请回答下列问题:
请回答下列问题: (1)Z2+ 的核外电子排布式是 ,Z原子基态时简化电子排布式为 。
(1)Z2+ 的核外电子排布式是 ,Z原子基态时简化电子排布式为 。 (2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。
(2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。
| A.稳定性:甲>乙,沸点:甲>乙 | B.稳定性:甲>乙,沸点:甲<乙 |
C.稳定性:甲<乙,沸点:甲<乙 | D.稳定性:甲<乙,沸点:甲>乙 |
 (3)Q、R、Y三种元素的第一电离能数值由小到大的顺序为 (用元素符号作答)。
(3)Q、R、Y三种元素的第一电离能数值由小到大的顺序为 (用元素符号作答)。 (4)五种元素中,电负性最大与最小的两种非金属元素形成的化合物的化学式为 。
(4)五种元素中,电负性最大与最小的两种非金属元素形成的化合物的化学式为 。 (5)Q的一种氢化物相对分子质量为28,其中分子中的σ键与π键的键数之比为 ,该氢化物与氧气形成的燃料电池在碱性电解质中负极反应为 。
(5)Q的一种氢化物相对分子质量为28,其中分子中的σ键与π键的键数之比为 ,该氢化物与氧气形成的燃料电池在碱性电解质中负极反应为 。
.氯化铍是用于制有机铍化合物和金属铍的重要原料。
(1)BeCl2分子中组成元素Be的基态原子的价电子排布式为,其元素的第一电离能B元素(填“>”或“<” 或“=”),原因是。
(2)已知BeCl2加热易升华,液态BeCl2不导电,BeCl2晶体类型为; BeCl2中Be原子的杂化轨道类型是。
(3)Kraus用阴离子树脂交换法提取一种组成元素为氯和铍的阴离子,该阴离子内铍原子达到8电子稳定结构,则该离子内存在的微粒间的作用力是,阴离子的结构式为。
、氮化硅是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定。工业上普遍采用高纯硅与纯氮在1300℃反应获得氮化硅。
(1)根据性质,推测氮化硅属于________晶体。
(2)根据性质,推测氮化硅陶瓷的用途是_________(填序号)。
| A.制汽轮机叶片 | B.制有色玻璃 |
| C.制永久性模具 | D.制造柴油机 |
(3)根据化合价规律,推测氮化硅的化学式为_________。
(4)氮化硅陶瓷抗腐蚀性强,除氢氟酸外,它不与其他无机酸反应。试写出该陶瓷被氢氟酸腐蚀的化学方程式_______________________________________。
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为。
(2)B的氢化物的分子空间构型是。其中心原子采取杂化
(3)写出化合物AC2的电子式;一种由B、C组成的化合物与AC2互为等电子体,其化学式为。
(4)ECl3与B、C的氢化物形成配位数为六的配合物的化学式为。
短周期元素X、Y、Z在周期表中位置关系如图:(答题时,X、Y、Z用所对应的元素符号表示)
| X |
||
| Y |
||
| Z |
(1)x元素的单质分子式是_______,单质是_______晶体。
(2)自然界中存在一种仅含钙与Y两种元素的天然矿物,其电子式为_______,属于_______晶体。
(3)Z的氢化物和Y的氢化物沸点高低顺序是:,理由:。
(4)X、Y、Z三种元素中,电负性最大的是:。
乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1)CaC2与水反应生成乙炔的化学方程式;
CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为_________________________。
(2)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是;分子中处于同一直线上的原子数目最多为。
(3)金刚石的晶胞如图所示,已知六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,立方氮化硼晶体密度为ag/cm3,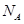 表示阿伏加德罗常数,则立方氮化硼晶胞体积为cm3。
表示阿伏加德罗常数,则立方氮化硼晶胞体积为cm3。