影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。实验药品:铜、铁、镁、0.5mol/LH2SO4、2mol/LH2SO4、、18.4mol/LH2SO4
A:甲同学研究的实验报告如下表:
| 实验步骤 |
现象 |
结论 |
| ①分别取等体积的2mol/L的硫酸于试管中 ② |
反应速率镁>铁,铜不反应 |
金属的性质越活泼,反应速率越快 |
(1)甲同学表中实验步骤②为 。
(2)甲同学的实验目的是 ;要得出正确的实验结论,还需控制的实验条件是 。B:乙同学为了更精确的研究浓度对反应速率的影响,利用下图所示装置进行实验
(3)乙同学在实验中应该测定的数据是 。
(4)乙同学完成该实验应选用的实验药品 。该实验中不选用某浓度的硫酸,理由是 。
(1)实验室可用甲酸与浓硫酸共热制备一氧化碳:HCOOH浓硫酸========H2O+CO↑,实验的部分装置如下图所示。制备时先加热浓硫酸至80℃—90℃,再逐滴滴入甲酸。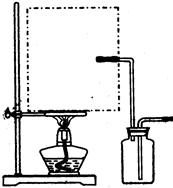

Ⅰ制备COⅡⅢ收集CO
①从下图挑选所需的仪器,画出Ⅰ中所缺的气体发生装置(添加必要的塞子、玻璃管、胶皮管,固定装置不用画),并标明容器中的试剂。




分液漏斗长颈漏斗蒸馏烧瓶集气瓶温度计
②装置Ⅱ的作用是。
(2)实验室可用甲酸制备甲酸铜。其方法是先用硫酸铜和碳酸氢钠作用制得碱式碳酸铜,然后再与甲酸斥制得四水甲酸铜[Cu(HCOO)2·4H2O]晶体。相关的化学方程式是:
2CuSO4+4 NaHCO3="=" Cu(OH)2·CuCO3↓+3CO2↑+2Na2SO4+H2O
Cu(OH)2·CuCO3+4HCOOH+ 5H2O="=2" Cu(HCOO)2·4H2O+ CO2↑
实验步骤如下:
Ⅰ、碱式碳酸铜的制备: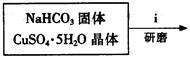
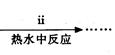
③步骤ⅰ是将一定量CuSO4·5H2O晶体和NaHCO3固体一起放到研钵中研磨,其目的是。
④步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃—80℃,如果看到(填写实验现象),说明温度过高。
Ⅱ、甲酸铜的制备:
将Cu(OH)2·CuCO3固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。在通风橱中蒸发滤液至原体积的1/3时,冷却析出晶体,过滤,再用少量无水乙醇洗涤晶体2—3次,晾干,得到产品。
⑤“趁热过滤”中,必须“趁热”的原因是。
⑥用乙醇洗涤晶体的目的是。
某钠盐溶液可能含有阴离子NO3-、CO32-、SO32-、SO42-、Cl-、Br-、I-、为鉴别这些离子,分别取少量溶液进行以下实验:
①测得混合液呈碱性;
②加HCl后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
③加CCl4后,滴加少量氯水,振荡后,CCl4后层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
(1)分析上述5个实验,写出每一步实验鉴定离子的结论与理由。
实验① ;
实验② ;
实验③ ;
实验④ ;
实验⑤ ;
(2)上述5个实验不能确定是否存在的离子是 。
(3)检验钠离子的方法是 。
实验室制取溴乙烷的反应如下:NaBr+H2SO4====NaHSO4+HBr,CH3CH2OH+HBr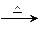 CH3CH2Br+H2O。已知反应物的用量NaBr(s)0.3mol,乙醇0.25 mol,浓硫酸36 mL(98%,密度1.84 g·cm-3),水25 mL,其中乙醇的密度约为水的密度的4/5,试回答:
CH3CH2Br+H2O。已知反应物的用量NaBr(s)0.3mol,乙醇0.25 mol,浓硫酸36 mL(98%,密度1.84 g·cm-3),水25 mL,其中乙醇的密度约为水的密度的4/5,试回答:
(1)反应时,若温度过高,可有红棕色气体产生,写出反应的化学方程式:_____________________________________。
(2)从棕黄色的粗溴乙烷制取无色的溴乙烷,应加入的试剂是____________,必须使用的仪器是__________________。
(3)本实验的产率为60%,则可制取溴乙烷____________g。
溴乙烷是一种难溶于水的无色液体,密度约为水的1.5倍,沸点为38.4 ℃。实验室制取溴乙烷的反应如下:
NaBr+H2SO4 NaHSO4+HBr
NaHSO4+HBr
CH3CH2OH+HBr CH3CH2Br+H2O
CH3CH2Br+H2O
已知反应物的用量,NaBr(固体)0.3 mol,乙醇0.25mol,浓硫酸36 mL(98%,密度1.84 g·cm-3),水25 mL,其中乙醇的密度约为水的密度的4/5。试回答:
图6-2
(1)仅用图6-2所示仪器安装制取和收集溴乙烷的装置,要求达到安全、损失少、不污染环境的目的,有关仪器的选择和连接顺序为(填数字)____________。
(2)写出不能选用的仪器(填仪器代码,如甲、乙……)及理由。
| 不能选用的仪器 |
理由 |
(3)反应时,若温度过高,可见有棕色气体产生,写出反应的化学方程式:_________。
(4)从棕黄色的粗溴乙烷制取无色的溴乙烷,应加入的试剂是_________,必须使用的仪器是_________。
(5)本实验的产率为60%,则可制取溴乙烷_________g。
1,2-二溴乙烷可作汽油抗爆剂的添加剂。常温下,它是无色液体,密度为2.18 g·cm-3,沸点131.4 ℃,熔点9.79 ℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2-二溴乙烷。图中:分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液;试管d中装有液溴(表面覆盖少量水)。
(1)写出本题中涉及的两个化学反应方程式:。
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时安全瓶b中的现象:______________________________________________________________。
(3)容器c中NaOH溶液的作用是__________________________________________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因。