已知乙酸(HA)的酸性比甲酸(HB)弱,在物质的量浓度均为0.1 mol/L的NaA和NaB混合溶液中,下列排序正确的是()
A.c(OH-)>c(HA)>c(HB)>c(H+) B.c(OH-)>c(A-)>c(B-)>c(H+)
C.c(OH-)>c(B-)>c(A-)>c(H+) D.c(OH-)>c(HB)>c(HA)>c(H+)
pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH仍相同,则m和n的关系是()
| A.m=n | B.m>n | C.m<n | D.无法判断 |
如图所示,a,b,c,d均为石墨电极,通电进行电解,下列说法正确的是()
A.乙池中d的电极反应为 |
| B.a,c两极产生气体的物质的量相等 |
| C.甲、乙两池中溶液pH均保持不变 |
D.乙池中发生的反应为  |
已知热化学方程式: ,则对于热化学方程式:
,则对于热化学方程式: ,下列说法正确的是()
,下列说法正确的是()
| A.热化学反应方程式中化学计量数表示分子个数 |
B.该反应的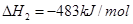 |
C. |
D.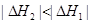 |
反应C(s)+H2O(g) = CO(g)+H2(g)在一
可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是()
①增加C的量②将容器的体积缩小一半
③保持体积不变,充入N2④保持压强不变,充入N2
| A.①④ | B.①③ | C.③ | D.②③ |