现有下列4种物质:① NH3、② NO2、③ NaCl溶液、④ Na2CO3溶液。其中,
常温下为红棕色的气体是 (填序号,下同),能使湿润的红色石蕊试纸变蓝的气体是 ,与盐酸反应能生成气体的溶液是 ,加入硝酸银溶液生成白色沉淀,滴加稀硝酸沉淀不消失的溶液是 。
周期表前20号元素中有A、B、C、D、E五种元素。已知它们都不是稀有气体元素且只有一种金属元素,且原子半径依次减小,其中除了A和E同族外其他都不同族,A与C、B与E原子的电子层数都相差2,A、B原子最外层电子数之比为1:4。
(1)写出元素符号:BDE
(2)A和C能以原子数1:1形成一种化合物,写出该化合物的化学式
某化合物是科学家制备的一种重要的化合物,与水反应可产生一种使湿润的红色石蕊试纸变蓝的气体。将这种化合物在无色火焰上灼烧可使火焰呈黄色,且组成这种化合物的两种粒子具有相同的电子层结构。请回答下列问题:
(1)该化合物的化学式是,是由键构成。
(2)该化合物与盐酸反应生成种盐,写出对应的化学方程式
写出下列为物质的电子式:
O(原子) H2S CaCl2 NaOH HClO
已知A的分子式为C3H4O2,下图是A~H间相互转化的关系图,其中F中含有一个七元环;H是一种高分子化合物。(提示:羟基与双键碳原子相连的醇不存在;同一个碳原子上连有2个或多个羟基的多元醇不存在)请填写下列空白: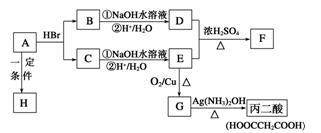
(1)A中含有的官能团有(写结构简式)。
(2)请写出下列有机物的结构简式:C;F。
(3)请指出下列反应的反应类型:A—→B; C—→E。
(4)G中不同化学环境的氢原子有种。
(5)请写出下列反应的化学方程式:
①A—→H;②B—→D(第①步)__。
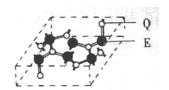
有E、Q、T、X、Z五种前四周期元素,原子序数E<Q<T<X<Z。E、Q、T三种元素的基态原子具有相同的能层和能级,且I1(E)<I1(T)<I1(Q),其中基态Q原子的2p轨道处于半充满状态,且QT2+与ET2互为等电子体。x为周期表前四周期中电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
(1)写出QT2+的电子式,基态Z原子的核外电子排布式为。
(2)Q的简单氢化物极易溶于T的简单氢化物,其主要原因有(写两条)。
(3)ET2的空间构型为,为分子(填“极性”或“非极性”)
(4)化合物甲由T、X两元素组成,高温下,化合物甲晶体呈立方体结构,其晶胞如图,甲的化学式为。晶体中氧的化合价部分为0价,部分为-2价,则下列说法正确的是()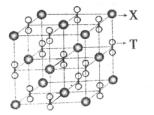
| A.每个晶胞中含有14个心和13个O2- |
| B.晶体中每个K+周围有8个O2-,每O2-周围有8个K+ |
| C.晶体中与每个K距离最近的K+有8个 |
| D.晶体中,O价氧原子与-2价氧原子的数目比为3:l |
(5)化合物乙的晶胞如图,乙由E、Q两元素组成,硬度超过金刚石。则乙的晶体中E、Q两种元素原子的 杂化方式均为。
杂化方式均为。