下列图示的实验操作中,正确的是( )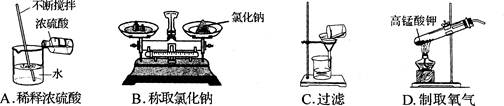
TiO2在光照射下可使水分解:2H2O 2H2↑+O2↑,该过程类似植物的光合作用。下图是光照射下TiO2分解水的装置示意图。下列叙述正确的是 ( )
2H2↑+O2↑,该过程类似植物的光合作用。下图是光照射下TiO2分解水的装置示意图。下列叙述正确的是 ( )
| A.该装置可以将光能转化为电能,同时也能将其转化为化学能 |
| B.TiO2电极上发生的反应为:2H++2e-=H2↑ |
| C.该装置工作时,电流由TiO2电极经R流向铂电极 |
| D.该装置工作时,TiO2电极附近溶液的pH变大 |
将甲、乙两种金属的性质相比较,已知①甲跟水反应比乙跟水反应剧烈;②甲单质能从乙的盐溶液中置换出乙单质;③甲的最高价氧化物对应水化物的碱性比乙的最高价氧化物对应水化物的碱性强;④与某金属反应时甲原子得电子数目比乙的多;⑤以甲、乙两金属为电极构成原电池,甲作负极。能说明甲的金属性比乙强的是( )
| A.①②③ | B.③⑤ | C.①②③⑤ | D.①②③④⑤ |
有关如下图所示原电池的叙述,正确的是(盐桥中装有含琼脂的KCl饱和溶液) ( )
| A.反应中,盐桥中的K+会移向CuSO4溶液 |
| B.取出盐桥后,电流计依然发生偏转 |
| C.铜片上有气泡逸出 |
| D.反应前后铜片质量不改变 |
下列叙述正确的是 ( )
①原电池是把化学能转化成电能的一种装置 ②原电池的正极发生氧化反应,负极发生还原反应 ③不能自发进行的氧化还原反应,通过原电池的装置均可实现 ④碳棒不能用来作原电池的正极 ⑤反应Cu+2Ag+=2Ag+Cu2+,能以原电池的形式来实现
| A.①⑤ | B.①④⑤ | C.②③④ | D.②⑤ |
根据下列热化学方程式:
(1)C(s)+O2(g)=CO2(g) ΔH1=-393.5 kJ·mol-1
(2)H2(g)+ O2(g)=H2O(l) ΔH2=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH2=-285.8 kJ·mol-1
(3)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH3=-870.3 kJ·mol-1
可以计算出2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为 ( )
| A.ΔH=+244.1 kJ·mol-1 |
| B.ΔH=-488.3 kJ·mol-1 |
| C.ΔH=-996.6 kJ·mol-1 |
| D.ΔH=+996.6 kJ·mol-1 |