某温度下,反应2NO2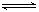 N2O4;△H<O,在密闭容器中达到平衡。平衡时改变外界条件,使反应再次平衡,新平衡时,c(NO2)/c(N2O4)与原平衡相比变大了,则改变条件的可能有
N2O4;△H<O,在密闭容器中达到平衡。平衡时改变外界条件,使反应再次平衡,新平衡时,c(NO2)/c(N2O4)与原平衡相比变大了,则改变条件的可能有
| A.保持容器容积和温度不变,向容器内补充了NO2 |
| B.保持容器压强和温度不变,向容器内补充了N2O4 |
| C.保持容器容积和温度不变,向容器内补充了N2 |
| D.保持容器的容积不变,升高了温度 |
对于反应A2+3B2 2C来说,以下化学表示的反应速率最快的是()
2C来说,以下化学表示的反应速率最快的是()
A.v(B2)="0.8" mol·L-1·s-1 B. v(B2)="0.42" mol·L-1·s-1
C.v(C)="0.6" mol·L-1·s-1 D. v(A2)="0.4" mol·L-1·s-1
温度不变,在恒容的容器中进行下列反应:N2O4(g)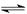 2NO2(g),若N2O4的浓度由0.1 mol· L-1降到0.07 mol· L-1需要15 s,那么N2O4的浓度由0.07 mol·L-1降到0.05 mol·L-1所需反应的时间()
2NO2(g),若N2O4的浓度由0.1 mol· L-1降到0.07 mol· L-1需要15 s,那么N2O4的浓度由0.07 mol·L-1降到0.05 mol·L-1所需反应的时间()
| A.大于10 s | B.等于10 s | C.等于5 s | D.小于10 s |
我国拥有完全自主产权的氢氧燃料电池车在奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。下列有关电池的叙述不正确的是()
| A.正极反应式为:O2+2H2O+4e- ="=" 4OH- |
| B.用该电池电解CuCl2溶液,产生2.24LCl2(标况)时,有0.1mol电子转移 |
| C.该燃料电池的总反应方程式为:2H2+O2==2H2O |
| D.工作一段时间后,电解液中的KOH的物质的量不变 |
下列反应达到平衡后,加压或升温,平衡都向正反应方向移动的是()
A.2NO2(g) N2O4(g) △H<0 N2O4(g) △H<0 |
B.3O2(g) 2O3(g)△H>0 2O3(g)△H>0 |
C.H2(g)+I2(g) 2HI(g)△H<0 2HI(g)△H<0 |
D.NH4HCO3(s) NH3(g)+H2O(g)+CO2(g) △H>0 NH3(g)+H2O(g)+CO2(g) △H>0 |
对于达到平衡的反应:2A(g)+B(g) nC(g),符合右图所示的结论是()
nC(g),符合右图所示的结论是()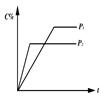
| A.P1>P2,n>3 | B.P1>P2,n<3 |
| C.P1<P2,n>3 | D.P1<P2,n<3 |