以NA表示阿伏加德罗常数,下列说法错误的是( )
| A.标准状况下,22.4LCH4和CH3Cl的混合物所含有的分子数目为NA |
| B.7.8g Na2O2晶体中含有阴阳离子总数为0.4NA |
| C.1 mol SiO2晶体中含有4NA Si–O键 |
| D.1.4 g乙烯(C2H4)和丙烯(C3H6)的混合物中含碳氢键数为0.2 NA |
在密团容器中充入1molCO和1molH2O(气),在一定条件下达到平衡时生成了2/3mol CO2(反应为CO+H2O(g)  CO2+H2),当其他条件不变,充入的水蒸气改变为2mol时,平衡时生成CO2的物质的量可能是
CO2+H2),当其他条件不变,充入的水蒸气改变为2mol时,平衡时生成CO2的物质的量可能是
| A.0.5mol | B.0.95mol | C.1mol | D.2/3mol |
常温下的定容容器中,建立如下平衡:3NO2+H2O NO+2HNO3,在其他条件不变时,若往容器中通入少量的氧气后、原体系将会发生的变化是
NO+2HNO3,在其他条件不变时,若往容器中通入少量的氧气后、原体系将会发生的变化是
| A.平衡向逆反应方向移动 |
| B.NO的物质的量可能不变 |
| C.NO的物质的量一定会减少 |
| D.NO2增加的物质的量是通入O2的物质的量的2倍 |
一定条件反应N2+3H2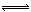 2NH3达平衡,当单独改变下述条件后有关叙述错误
2NH3达平衡,当单独改变下述条件后有关叙述错误
| A.加催化剂,v(正)和v (逆)都发生变化,且变化的倍数相等 |
| B.加压, v (正)和v (逆)都增大,且v (正)增加倍数大于v (逆)增加倍数 |
| C.降温, v (正)和v (逆)都减少,且v (正)减少倍数大于v (逆)减少倍数 |
| D.增加N2的浓度, v (正)和v (逆)都增大,且v (正)增加倍数大于v (逆)增加倍数 |
甲萘醌(维生素K)有止血作用,它可通过2—甲基萘的氧化而制得,反应中常用乙酸作催化剂,该反应放热,可表示为: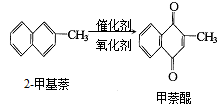
在某次合成反应中,用1.4g的2—甲基萘,才制得0.17g甲萘醌,已知该次合成反应的速率是快的,试判断导致其产率低的原因是
| A.使用了过量的氧化剂 | B.没有用乙酸,而是使用了其它催化剂 |
| C.把反应混合物加热 | D.所生成的甲萘醌是沉淀物 |
在密闭容器中有可逆反应:nA(g) +mB(g)  pC(g) △H >O处于平衡状态(又知n+m>P),则下列说法正确的是①升高温度时,c(B)/C(C)的比值减小②降温时体系内混合气体平均相对分子质量减小③加入B,A的转化率变大④加入催化剂,气体的总物质的量不变⑤充入C,则A、B的物质的量增大
pC(g) △H >O处于平衡状态(又知n+m>P),则下列说法正确的是①升高温度时,c(B)/C(C)的比值减小②降温时体系内混合气体平均相对分子质量减小③加入B,A的转化率变大④加入催化剂,气体的总物质的量不变⑤充入C,则A、B的物质的量增大
A.③④ B.①②⑤ C.②③⑤D.全部