下列有关晶体的说法中一定正确的是( )
①原子晶体中只存在非极性共价键
②稀有气体形成的晶体属于原子晶体
③干冰晶体升华时,分子内共价键会发生断裂
④金属元素和非金属元素形成的化合物一定是离子化合物
⑤分子晶体的堆积均为分子密堆积
⑥金属晶体和离子晶体都能导电
⑦离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键
⑧依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体
| A.①③⑦ | B.只有⑦ | C.②④⑤⑦ | D.⑤⑥⑧ |
实验式相同,但既不是同系物,又不是同分异构体的是( )
| A.1戊烯和2甲基1丙烯 | B.甲醛和甲酸甲酯 |
| C.1丁醇与甲乙醚 | D.丙酸和甲酸乙酯 |
下列关于同分异构体异构方法的说法中,正确的是( )
A.CH3CH2CH2CH3和CH3CH(CH3)2属于碳键异构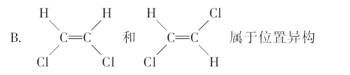
C.CH2===C(CH3)2和CH3CH===CHCH3属于官能团异构
D.CH3CH2CH2COOH和CH3COOCH2CH3属于位置异构
下列关于有机物的叙述中正确的是( )
| A.两种有机物若具有相同的相对分子质量,不同的结构,则一定互为同分异构体 |
| B.实验证明,不存在两种邻二甲苯,所以现代物质结构理论认为苯分子中的碳碳键完全相同而不是单双键交替的结构 |
| C.等质量的两种有机物完全燃烧生成等质量的水,则两种有机物一定具有相同的最简式 |
| D.两种有机物不论以何种物质的量比混合,只要总物质的量不变,消耗的氧气和生成的水的量也不变,则两种有机物必定具有相同的分子组成 |
已知酸式盐NaHB在水溶液中存在下列反应:①NaHB===Na++HB-,②HB-===H++B2-,③HB-+H2O===H2B+OH-,且溶液中c(H+)>c(OH-),则下列说法一定正确的是( )
| A.NaHB为强电解质 |
| B.H2B为强酸 |
| C.NaHB溶液中仅存在HB-、B2-两种含B元素的离子 |
| D.HB-的电离程度小于HB-的水解程度 |
常温下,水的离子积为Kw,下列说法正确的是( )
| A.在pH=11的溶液中,水电离出的c(OH-)一定等于10-3 mol/L |
| B.将pH=1的酸和pH=13的碱溶液等体积混合后,溶液的pH一定等于7 |
| C.将物质的量浓度和体积都相同的一元酸HA与一元碱BOH混合后,溶液呈中性,则反应后溶液中c(H+)= |
| D.若强酸、强碱中和后溶液的pH=7,则中和之前酸、碱的pH之和一定等于14 |