关于氢键的下列说法中不正确的是( )
| A.冰中平均每个水分子可形成2个氢键 |
| B.分子间氢键使物质熔点和沸点升高 |
| C.分子间形成氢键可使物质在水中的溶解度增大 |
| D.HF的稳定性很强,是因为其分子间能形成氢键 |
将过量的铝粉与FeO·2Fe2O3粉末配制成铝热剂,并分成两等份。一份直接放入足量的烧碱溶液中,充分反应后放出气体15.68 L(标准状况);另一份在高温下发生铝热反应,反应后的混合物与足量的盐酸反应,放出气体的体积(标准状况)可能为
| A.11.20 L | B.15.68 L | C.22.40 L | D.13.36 L |
在碘酸钠(NaIO3)的碱性溶液中通入氯气,可以得到高碘酸钠(Na2H3IO6)。下列有关该反应的说法错误的是
| A.在该反应中碘酸钠作还原剂 |
| B.碱性条件下,氯气的氧化性强于高碘酸钠 |
| C.反应中生成1 mol Na2H3IO6,转移2 mol电子 |
| D.反应中氧化产物与还原产物的物质的量之比为2 : 1 |
现有两种不含结晶水的盐,它们在不同温度下的溶解度如下表:
| 20℃ |
50℃ |
|
| A的溶解度 |
35.7 g |
46.4 g |
| B的溶解度 |
31.6 g |
108 g |
下列说法中,正确的是
A.可采用重结晶法使A、B混合物分离
B.A的溶解度一定大于B的溶解度
C.20℃时,无法配制30%的A的不饱和溶液
D.将208 g B的饱和溶液降温到20℃,析出76.4 g B
氧可与许多元素形成化合物,下列有关叙述错误的是
| A.氧与氟形成的化合物分子式为OF2 |
| B.次氯酸分子的结构式为H-Cl-O |
C.Na2O2的电子式为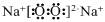 |
D.在MgO晶体中,O2-的结构示意图可表示为 |
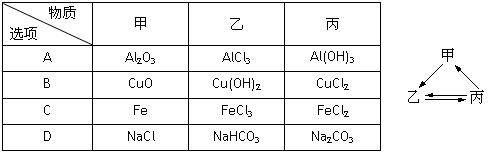
下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是