下列实验设计方案中,可行的是 ( )
| A.用加入过量CuCl2溶液,再过滤,除去Cu(NO3)2溶液中混有的AgNO3 |
| B.用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体 |
| C.向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液中的SO42— |
| D.先后添加石蕊试液、BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开 |
下列各组离子以适当比例混合,可以形成无色透明碱性溶液的是
| A.Na+、 Ba2+、OH-、SO42- | B.Ag+、NH4+、OH-、NO3- |
| C.Mg2+、Na+、AlO2-、OH- | D.MnO4-、Al3+、SO42-、Cl- |
下列离子方程式正确的是
A.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2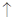 |
| B.FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+ |
C.向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性:Ba2++OH-+H++SO42-=BaSO4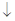 +H2O +H2O |
D.用小苏打类药物治疗胃酸过多:HCO3-+H+=CO2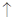 +H2O +H2O |
下列物质中,分子物质的量最多的是(相对原子质量 H—1 O—16)
| A.1molN2 | B.1g H2 | C.0.1NAO2 | D.4℃时,20mL水 |
下列物质的分类正确的是
| 碱 |
酸 |
盐 |
碱性氧化物 |
酸性氧化物 |
|
| A |
NaOH |
H2SO4 |
BaCO3 |
SO2 |
CO2 |
| B |
NaOH |
HCl |
NaCl |
Na2O |
CO |
| C |
NaOH |
CH3COOH |
CaCl2 |
CO |
SO2 |
| D |
KOH |
HNO3 |
CaCO3 |
CaO |
SO3 |
下列有关微粒或物质的“量”的叙述不正确的是
| A.浓度分别为2 mol/L和1 mol/L的Na2CO3溶液中,C(CO32一)的比值为2:1 |
| B.常温常压下,16 g 02和O3混合气体中含有NA个氧原子 |
| C.46 g NO2和N204混合气体的物质的量之和大于O.5 mol,小于l mol |
| D.向饱和CuS04溶液中加入1 mol CuS04固体,则析出的晶体的质量大于250 g |