随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
(1)处理NOx的一种方法是利用甲烷催化还原NOx。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为 。
(2)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:2NO(g)+2CO(g) N2(g)+2CO2(g);△H<0。若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示,该反应的化学平衡常数为K= 。若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将 移动(填“向左”、 “向右”或“不”)。
N2(g)+2CO2(g);△H<0。若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示,该反应的化学平衡常数为K= 。若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将 移动(填“向左”、 “向右”或“不”)。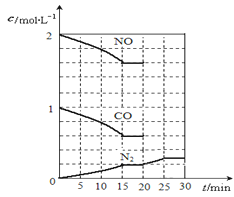
20min时,若改变反应条件,导致N2浓度发生如图11所示的变化,则改变的条件可能是
(填序号)。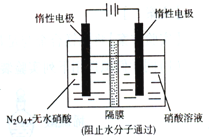
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的量
(3)肼(N2H4)用亚硝酸氧化可生成氮的另一种氢化物,该氢化物的相对分子质量为43.0,其中氮原子的质量分数为0.977。写出肼与亚硝酸反应的化学方程式 。
(4)如图所示装置可用于制备N2O5,则生成N2O5的那一极电极反应式为 。
由Cu、N、B、Ni等元素组成的新型材料有着广泛用途。
(1)基态Cu+的最外层核外电子排布式为_________。
(2)研究者预想合成一个纯粹由氮组成的新物种N5+N3-,若N5+中每个氮原子均满足8电子结构,以下有关N5+推测正确的是。
A.N5+有24个电子
B.N5+离子中存在三对未成键的电子对
C.N5+阳离子中存在两个氮氮三键
(3)化合物A(H3BNH3)是一种潜在的储氢材料,它可由六元环状化合物 (HB=NH)3。通过3CH4 +2(HB=NH)3+6H2O ==3CO2+6H3BNH3制得。
①与上述化学方程式有关的叙述不正确的是_________。(填标号)
A.反应前后碳原子的轨道杂化类型不变
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
C.第一电离能:N>O>C>B
D.化合物A中存在配位键
②1个(HB=NH)3分子中有_________个σ键。
(4)在硼酸盐中,阴离子有链状、环状等多种结构形式。图(a)是一种链状结构的多硼酸根,则多硼酸根离子符号为_________。图(b)是硼砂晶体中阴离子的环状结构,其中硼原子采取的杂化类型为_________。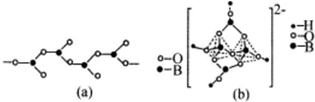
(5) NiO晶体结构与NaCl晶体类似,其晶胞的棱长为acm,则该晶体中距离最近的两个阳离子核间的距离为_________(用含有a的代数式表示)。在一定温度下,NiO晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为_________g(氧离子的半径为1. 40×10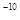 m,
m, ≈l. 732)。
≈l. 732)。
(有机化学基础选做题,共9分)
(1)写出葡萄糖发生银镜反应的化学方程式___________________。
(2)某有机物含C、H、O三种元素,它的红外吸收光谱表明有羟基O-H键和烃基上C-H键的红外吸收峰,且烃基与羟基上氢原子个数之比为2:1,它的相对分子质量为62,则该有机物的结构简式为__________。
(3)向苯酚钠溶液中通入少量的CO2 ,溶液将变浑浊,请写出反应的化学方程式_____________。
(4)某有机物的结构简式如图, 则此有机物可发生的反应类型有______(填字母)
则此有机物可发生的反应类型有______(填字母)
①取代反应②加聚反应③消去反应④酯化反应⑤水解反应⑥氧化反应⑦显色反应
A.①②④⑥⑦B.②③④⑥⑦C.①②③④⑤⑥D.全部
(物质结构与性质选做题,共9分)碳、氮、氧的单质及其化合物在自然界中广泛存在。
(1)基态碳原子的价电子排布图可表示为_____________。
(2)碳、氮、氧原子第一电离能由大到小的顺序是: _________________。
(3)冰晶胞中水分子的空间排列方式与金刚石晶胞类似。每个冰晶胞平均占有________个水分子。
(4)请写出一个反应方程式以表达出反应前碳原子的杂化方式为sp2,反应后变为sp3:__________。
(5)写出CO分子的一种等电子体的分子式__________。
(本题共12分)硫及氯的化合物在生产及生活中有着广泛的应用。
(1)SO2和Cl2均可作漂白剂,但将它们按物质的量1:1通入水中,却没有漂白性,原因是_________(写出反应的离子方程式)。
(2)工业上常用电解法制Cl2,写出反应的化学方程式_______________。
(3)某同学将足量的SO2通入一支装有氯化钡溶液的试管中,未见沉淀生成。向该试管中加入足量________(填字母),便能产生沉淀。
| A.氨水 | B.稀盐酸 | C.硝酸钾溶液 | D.氯水 |
(4)将22.4L(标准状况)的SO2气体通入1L1 mol·L-1的NaOH溶液中,所得溶液中离子浓度由大到小的顺序是______________。
(5)在25 ℃时,向0.1 L 0.002 mol·L-1的NaCl溶液中逐滴加入0.1 L 0.002 mol·L-1硝酸银溶液,有白色沉淀生成,向反应后的浊液中继续加入0.1 L 0.002 mol·L-1的NaI溶液,看到的现象是________,产生该现象的原因是_____________(用离子方程式表示)。(已知:25 ℃时Ksp(AgCl)=1.6×10-10,Ksp(AgI)=1.5×10-16)
海洋资源的利用具有广阔前景。
(1)下列不属于海水淡化的方法___________________(填序号)。
A.蒸馏法 B.离子交换法 C.过滤法 D.电渗析法
(2)下图是从海水中提取镁的简单流程。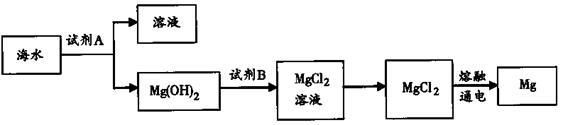
①试剂B是________(填化学式)。
②由无水MgCl2制取Mg的化学方程式是________________________。
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示: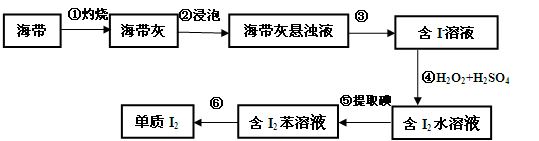
I:下列不属于步骤①操作所用的仪器是 ________(填序号)。
A.酒精灯 B.漏斗C.坩埚 D.泥三角
II:步骤③的实验操作名称是__________。
III:④步骤反应的离子方程式________。
IV:请设计一种检验提取碘后的水溶液中是否含有碘单质的简单方法。