“神九”飞船的发射成功,标志着我国航天事业进入领先行业。
(1).燃料电池的发展和航天的需求密不可分。燃料电池不仅能量转换率高,而且以氢气和氧气为燃料的电池,电池反应生成的水还可供宇航员饮用。
①使用酸性电解质的氢氧燃料电池,负极的电极反应为 。
②美国的阿波罗登月飞船使用的是碱性氢氧燃料电池,正极的电极反应为
O2 + 2H2O + 4e- = 4OH-,负极的电极反应为 。
③下图是熔融碳酸盐燃料电池的工作原理示意图。
已知负极的电极反应为2 H2 – 4e-+ 2CO32- ="2" H2O +2CO2,
正极的电极反应为 。
(2).太阳能电池也为航天飞船提供了方便的能源。在航天飞船内H2O和O2的循环中,借助太阳能电池,可以通过电解水提供O2。若有4 mol电子发生转移,则在阳极上得到气体的体积(标准状况)是 L。
以下是25 ℃时几种难溶电解质的溶解度:
| 难溶电解质 |
Mg(OH)2 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
| 溶解度/g |
9×10-4 |
1.7×10-6 |
1.5×10-4 |
3.0×10-9 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子。例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可。
请回答下列问题:
(1)上述三个除杂方案都能够达到很好效果,Fe2+、Fe3+都被转化为(填名称)而除去。
(2)①中加入的试剂应选择为宜。
(3)②中除去Fe3+所发生的总反应的化学方程式为。
(4)下列关于方案③相关的叙述中不正确的是(填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
C.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+能大量存在
常温下,取0.2mol·L-1HCl溶液与0.2mol·L-1MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
(1)混合溶液中由水电离出的c(H+)0.2mol·L-1HCl溶液中由水电离出的c(H+)(填“大于”、“小于”或“等于”)。
(2)求出混合物中下列算式的精确计算结果:
c(H+)−c(MOH)=,c(Cl-)−c(M+)=。
(3)若常温下取0.2mol·L-1MOH溶液与0.1mol·L-1HCl溶液等体积混合,测得混合溶液的pH<7,说明MOH的电离程度(填“大于”、“小于”或“等于”) MCl的水解程度。混合后的溶液中各离子浓度由大到小的顺序为。
进入2013年以来,我国中东部地区多次遭遇大范围、长时间的雾霾天气。车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。
(1)活性炭可处理大气污染物NO。在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F。当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
①结合上表数据,写出NO与活性炭反应的化学方程式。
②计算上述反应T2℃时的平衡常数K2=。
③根据上述信息判断,温度T1和T2的关系是(填序号)。
a.无法比较b.T1>T2c.T1<T2
(2)车辆排放的NO和CO在催化剂作用下可发生反应生成N2和CO2。在一体积为1L的密闭容积中,加入0.40mol的CO和0.40mol的NO,反应中N2的物质的量浓度的变化情况如图所示,
计算从反应开始到平衡时,平均反应速率v(NO)=。
(10分)A和甲是来自石油和煤的两种基本化工原料,A是气态烃,甲是液态烃。B和D是生活中两种常见的有机物,F是高分子化合物。相互转化关系如图所示(已知:R—CHO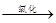 R—COOH)。
R—COOH)。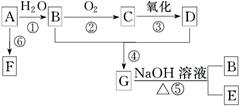
(1)A分子的电子式是____________。
(2)在反应①~⑥中,属于加成反应的是(填序号)。
(3)写出下列反应的化学方程式(有机物写结构简式)
②B→C:_______________________________________________________________;
④B+D→G:____________________________________________________________;
⑥A→F:________________________________________________________________。
镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。主要步骤如下: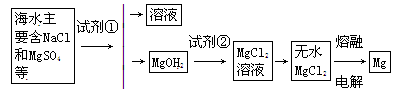
(1)为了使MgCl2转化为Mg(OH)2,试剂①可以选用。试剂②可以选用。
(2)验证MgCl2已完全转化为Mg(OH)2的方法是。
(3)由MgCl2溶液得到无水MgCl2的方法是。