以酚酞试液为指示剂,对某新制的NaOH溶液进行中和滴定试验,数据记录如下表:
| |
待测液 |
消耗标准盐酸 (0.10 mol/L)的体积 |
| ① |
20 mL NaOH溶液 |
V1 mL |
| ② |
20 mL NaOH溶液 +10 mL水 |
V2 mL |
| ③ |
敞开隔夜放置的 20 mLNaOH溶液 |
V3 mL |
该新制的NaOH溶液的浓度c mol/L合理的是( )
A.c=0.10×(V1+V2+V3)/(3×20)
B.c=0.10× (V1+V2)/(2×20)
C.c=0.10×(V1+V3)/(2×20)
D.c=0.10V1/20
下列有关仪器的使用正确的是
| A.将固体药品放在蒸发皿中进行高温焙烧 |
| B.六水氯化钙可用作食品干燥剂 |
| C.向试管中滴加液体时胶头滴管一定应悬于试管口的正上方 |
| D.冷凝管中冷却水的流向一定是下口进水、上口出水 |
下列离子方程式书写正确的是
A.实验室用MnO2和浓盐酸制取Cl2:MnO2+4HCl(浓) Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O |
| B.向NaHSO4溶液中滴加Ba(OH)2溶液至碱性:SO42-+2H++Ba2++2OH-=BaSO4↓+2H2O |
| C.石灰乳与Na2CO3溶液混合:Ca2++ CO32-=CaCO3↓ |
D.NH4Cl浓溶液中滴加浓NaOH溶液并加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
下列说法中正确的是
| A.胶体区别于其它分散系的本质特性是丁达尔效应 |
| B.利用半透膜可除去淀粉溶液中的少量NaCl |
| C.Fe(OH)3胶体带正电荷 |
| D.胶体能产生丁达尔效应的原因是胶粒使光线发生了折射 |
NA为阿伏加德罗常数的值。下列说法正确的是
| A.1.0L1.0mo1·L-1的NaAlO2水溶液中含有的氧原子数为2NA |
B.235g核素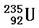 发生裂变反应: 发生裂变反应: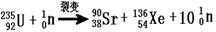 ,净产生的中子( ,净产生的中子(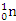 )数为10NA )数为10NA |
| C.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA |
| D.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
下列物质中,不属于电解质的是
| A.NaOH | B.H2SO4 | C.蔗糖 | D.NaCl |