过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用.它与二氧化碳反应的化学方程式为: 2Na2O2 + 2CO2 ="=" 2Na2CO3 + O2 。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:
(1)A中制取CO2 的装置,应从下列图①、②、③中选哪个图: 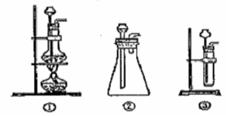
B装置的作用是 ,C装置内可能出现的现象是 。为了检验E中收集到的气体,在取出集气瓶后,
用 的木条伸入集气瓶内,木条会出现 。
(2)若E中的石灰水出现出现轻微白色浑浊,请说明原因: 。
(3)若D中的1.95g过氧化钠样品接近反应完毕时,你预测E装置内有何现象?
(4)你认为上述A-E的实验装置中,E部分是否安全、合理?E是否需要改为下列四项中的哪一项: 。(用甲、乙、丙、丁回答)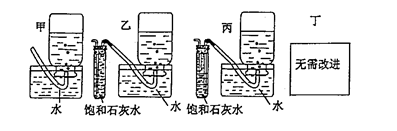
用图1-3所示装置(酒精灯、铁架台等未画出)制取三氯化磷。在具支烧瓶d中放入足量白磷,将氯气迅速而又不间断地通入具支烧瓶中,氯气与白磷就会发生反应,产生火焰。三氯化磷和五氯化磷的物理常数见下表。
| 熔点/℃ |
沸点/℃ |
|
| 三氯化磷 |
-122 |
76 |
| 五氯化磷 |
148 |
200 ℃分解 |
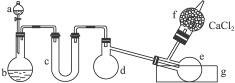
图1-3
(1)有浓盐酸、浓硫酸、白磷、二氧化锰、氢氧化钠等物质供选用,a、b中应该装入的试剂分别是:a________,b________。
(2)________(填仪器对应的字母)仪器需要加热。
(3)生成的三氯化磷在蒸馏烧瓶e中收集。为保证三氯化磷蒸气冷凝,应在水槽g中加入________。
(4)三氯化磷遇到水蒸气强烈反应,甚至发生爆炸,所以d、e仪器及装入其中的物质都不能含有水分。为除去氯气中的水分,c可以装入下列物质中的________(填字母)。
A.碱石灰 B.浓硫酸 C.无水氯化钙
(5)氯气和白磷反应放出大量的热,为使具支烧瓶d不致因局部过热而炸裂,实验开始前应在烧瓶的底部放少量________。
(6)实验室的白磷保存于水中,取出白磷后用滤纸吸干表面水分,浸入无水酒精中片刻,再浸入乙醚中片刻即可完全除去水分。已知水与酒精互溶,酒精与乙醚互溶,用上述方法可除去水的原因是________________________________________________________。
(7)为防止氯气污染空气,装置末端导出的气体最好用(填字母)________进行净化处理。
A.NaOH溶液 B.Ca(OH)2溶液 C.饱和食盐水
实验室合成氨的装置如图所示。试完成下列问题: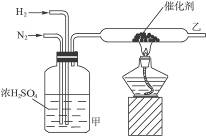
A装置甲的作用是①______________,②______________,③______________;从乙处导出的气体是;检验产物的简单化学方法是___________________________________________。
实验室常用饱和NaNO2与NH4Cl溶液反应制取纯净的氮气。反应方程式为
NaNO2+NH4Cl====NaCl+N2↑+2H2O(正反应放热)
如下图所示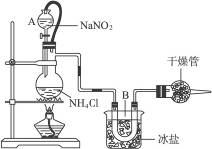
(1)装置中,A部分的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是______________(填写编号)。
a.防止NaNO2饱和溶液蒸发 b.保证实验装置不漏气 c.使NaNO2饱和溶液顺利滴下
(2)B部分的作用是_______________________。
a.冷疑 b.冷却氮气 c.缓冲氮气流
(3)加药品前必须进行的一个操作步骤是____________;加热片刻后即应移去酒精灯以防止反应物冲出,其原因是____________________________。
(4)收集N2前,必须进行的步骤是(用文字说明)__________________;收集N2最适宜的方法是(填写编号)______________。
a.用排气法收集在集气瓶中 b.用排水法收集在集气瓶中 c.直接收集在球胆或塑料袋中
微型化学实验具有装置小巧,节约药品,操作简便,现象明显,安全可靠,减少污染等特点,下图是某同学设计的NH3的催化氧化并检验反应生成的酸性物质的微型装置(图中必要的铁架台、铁夹、微型酒精灯等均略去)。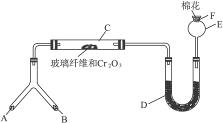
实验中所用试剂不超出下列范围:
①NH4Cl和Ca(OH)2的混合物②4∶1氨水③NaOH固体④KClO3和MnO2的混合物⑤蒸馏水⑥NH4HCO3固体⑦6 mol·L-1 NaOH溶液⑧0.5 mol·L-1 NaOH溶液⑨酚酞试液⑩碱石灰11浓H2SO412CuO
试完成下列问题:
(1)微型叉形管中液态物质A是__________,固体物质B是__________。
(2)C处发生反应的化学方程式是_______________________________________。
(3)混合物D是为了检验酸性物质的生成而放入的,其组成是__________,实验过程中的现象是_______________________。
(4)E处球形玻璃管的作用是________________________________________。
(5)F处的棉花应蘸取的物质是_________________________________,其反应的化学方程式是_____________________________________________________。
在进行研究性学习的过程中,学生发现等质量的铜片分别与等体积均过量的浓硝酸或稀硝酸反应,所得溶液(体积均相同)前者呈绿色,后者呈蓝色,针对这种现象,学生进行了讨论,出现两种意见:
一种认为Cu2+浓度差异引起了这种现象,你认为____________(填“正确”或“不正确”),依据是_______________________________________________________________________。
另一种意见是溶液呈绿色可能是Cu2+与NO2混合的结果,并用实验进行了证明,请简述实验方案与实验现象:_____________________________________________________________。